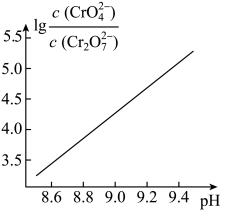
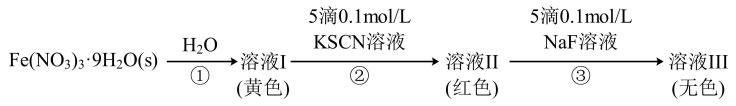
已知与
、
在溶液中存在以下平衡:
(红色);
(无色)
下列说法错误的是

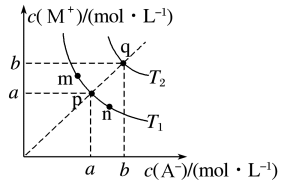

下列说法正确的是( )


CO(g)+H2O(g) ![]() CO2(g)+H2(g)ΔH=-akJ·mol-1(a>0)
CO2(g)+H2(g)ΔH=-akJ·mol-1(a>0)
相关反应数据如下:
| 容器 | 容器类型 | 起始温度/ | 起始物质的量/mol | 平衡时H2物质的量/mol | |||
| CO | H2O | CO2 | H2 | ||||
| Ⅰ | 恒温恒容 | 800 | 1.2 | 0.6 | 0 | 0 | 0.4 |
| Ⅱ | 恒温恒容 | 900 | 0.7 | 0.1 | 0.5 | 0.5 | |
| Ⅲ | 绝热恒容 | 800 | 0 | 0 | 1.2 | 0.8 | |
下列说法正确的是()

Ⅰ.制钠砂。向烧瓶中加入液体A和
金属钠,加热至钠熔化后,盖紧塞子,振荡至大量微小钠珠出现。
Ⅱ.制噻吩钠。降温至 , 加入
噻吩,反应至钠砂消失。
Ⅲ.制噻吩乙醇钠。降温至 , 加入稍过量的环氧乙烷的四氢呋喃溶液,反应
。
Ⅳ.水解。恢复室温,加入水,搅拌
;加盐酸调
至4~6,继续反应
, 分液;用水洗涤有机相,二次分液。
Ⅴ.分离。向有机相中加入无水 , 静置,过滤,对滤液进行蒸馏,蒸出四氢呋喃、噻吩和液体A后,得到产品
。
回答下列问题:
a.乙醇 b.水 c.甲苯 d.液氨
 )的原因是。
)的原因是。

A.低温低压B.低温高压C.高温低压D.高温高压

①下列说法正确的是。
A.可循环利用,
不可循环利用
B.过程ⅱ,吸收
可促使
氧化
的平衡正移
C.过程ⅱ产生的最终未被
吸收,在过程ⅲ被排出
D.相比于反应Ⅰ,该流程的总反应还原需吸收的能量更多
②过程ⅱ平衡后通入 , 测得一段时间内
物质的量上升,根据过程ⅲ,结合平衡移动原理,解释
物质的量上升的原因。
①常压下和
按物质的量之比
投料,某一时段内
和
的转化率随温度变化如图1,请在图2中画出
间R的变化趋势,并标明
时R值。

②催化剂X可提高R值,另一时段内转化率、R值随温度变化如下表:
|
温度/℃ |
480 |
500 |
520 |
550 |
|
|
7.9 |
11.5 |
20.2 |
34.8 |
|
R |
2.6 |
2.4 |
2.1 |
1.8 |
下列说法错误的是
A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率
B.温度越低,含氢产物中占比越高
C.温度升高,转化率增加,
转化率降低,R值减小
D.改变催化剂提高转化率,R值不一定增大

a.增大压强,化学平衡正向移动
b.增大浓度,正反应速率增大,逆反应速率减小
c.反应前的物质的量为
d.达到平衡时的转化率为

②若采用恒压,当温度高于后,
的转化率出现了断崖式下跌,原因可能是、(写出任意两点即可)。


项目 | 废水水质 | 排放标准 |
pH | 1.0 | 6~9 |
Cu2+含量/(mg•L-1) | 72 | ≤0.5 |
NH | 2632 | ≤15 |
资料2:Cu(OH)2+4NH3[Cu(NH3)4]2++2OH-
①根据实验结果分析,处理废水中Cu2+的最佳pH约为。
②结合资料解释实验结果图中b到d段曲线所示的过程。
C6H5C2H5(g)C6H5CH=CH2(g)+H2(g) ΔH=akJ•mol-1
保持气体总压不变,原料气按以下A、B、C三种投料方式进行:
A.乙苯
B.n(乙苯):n(N2)=1:10
C.n(乙苯):n(CO2)=1:10
三种投料分别达到平衡时,乙苯转化为苯乙烯的转化率[×100%]与温度的关系如图1所示。

①α0(填“>”、“<”或“不能确定”)。
②相同温度下,投料方式B乙苯的平衡转化率比投料方式A的高,其原因是。
③相同温度下,投料方式C乙苯的平衡转化率比投料方式B的高,其可能原因是。
④工业上利用“乙苯脱氢反应”生产苯乙烯时,会产生少量积碳。使用相同条件下的水蒸气代替N2 , 可较长时间内保持催化剂的催化活性,其原因是。
①在催化剂X作用下,CO2参与反应的机理如图2所示(α、β表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,B1、B2位点带部分负电荷)。根据元素电负性的变化规律,图2所示的反应机理中步骤I和步骤II可描述为。

②保持混合气体总压(p)等其他条件不变,CO2的分压[p(CO2)=×p]与乙苯转化率的关系如图3所示。p(CO2)>14kPa时,乙苯转化率下降的原因是。


i.
ii.
①已知相关键能数据如下表:
化学键 | ||||
键能/ | 436 | 464 | 803 | 1072 |
则反应i的。
②为了提高的产率,理论上应采用的措施是(填标号)。
A.低温低压 B.高温低压 C.高温高压 D.低温高压
③保持温度 , 压强
, 按投料比
向密闭容器中充入
和
, 反应相同时间测得不同催化剂下
转化率和
选择性的相关实验数据如下表所示(已知
选择性:转化的
中生成
的百分比)。
催化剂 |
|
|
cat。1 | 21.9% | 67.3% |
cat。2 | 36.1% | 100.0% |
上述条件下,使用cat。2作催化剂,下列说法能判断反应ii达到平衡状态的是(填标号)。
A.气体压强不再变化| B.气体平均相对分子质量不再变化
C.和
的物质的量之比为
D.
和
的物质的量之比不再变化

化学键 | ||||
键能 | 803 | x | 463 | 436 |

完成下列填空:
|
反应 |
平衡常数(25℃) |
活化能(kJ/mol) |
|
a: |
1.6×1057 |
3.17 |
|
b: |
6.2×1034 |
3.17 |
|
c: |
1.1×1041 |
58.17 |
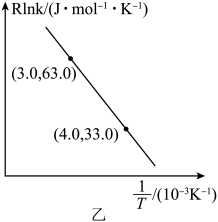
①已知: , 则
。
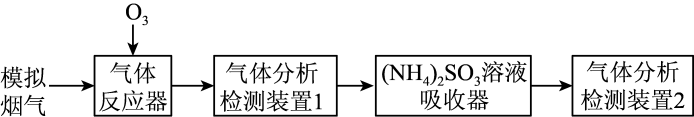
②其他条件不变,SO2和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内,SO2和NO的转化率随O3的浓度的变化如图。结合数据分析NO的转化率高于SO2的原因。


①(NH4)2SO3溶液显碱性,用化学平衡原理解释:。
②O3的浓度很低时,SO2的脱除率超过97%,原因是。
③在吸收器中,SO与NO2反应生成
和
的离子方程式是。
④在吸收器中,随着吸收过程的进行,部分被转化为N2 , 反应中
和N2的物质的量之比为1:1,该反应的离子方程式是。


其实验步骤为:称取工业烧碱2.088 g,配成500 mL溶液,取出25.00 mL,先加入25.00 mL 0.05 mol•L-1 BaCl2溶液(过量),然后滴入酚酞指示剂,再用0.1200 mol•L-1 的盐酸滴定至终点,平均消耗盐酸18.56 mL。
滴加BaCl2溶液时,反应的离子方程式为。计算该样品中NaOH的质量分数为。(用小数表示,保留至小数点后第3位),某次检测发现,实验值明显高于理论值,原因可能是。(选填编号)
a.工业烧碱已发生潮解 b.滴定管水洗后未用标准盐酸润洗
c.配制的待测液敞口放置时间过长 d.滴定时往锥形瓶中加水

已知:金属离子开始沉淀和完全沉淀的pH值如下表所示:
金属离子 | |||
开始沉淀的pH | 6.6 | 7.8 | 6.7 |
完全沉淀的pH | 9.2 | 10.4 | 9.5 |
回答下列问题:

电解时,各金属离子还原为单质的电压如下表:
金属离子 | |||
还原为单质的电压/V | 0.280 | 1.185 | 0.257 |
若要改进工艺,更好分离金属离子,应在(填字母)流程后开始使用电化学沉积法。最后析出的金属单质为。
A.“酸浸” B.“调pH” C.“沉镍” D.“沉锰”
与
的化学性质相似,在
溶液中逐滴加入
溶液直至过量,可观察到的现象是。

用离子方程式表示 溶液中的转化平衡。