①BaCl2、CuSO4、NaOH、NH4NO3
②Ba(NO3)2、NaCl、Na2SO4、H2SO4
③NaOH、FeCl3、MgSO4、KCl
④AgNO3、HCl、K2CO3、BaCl2
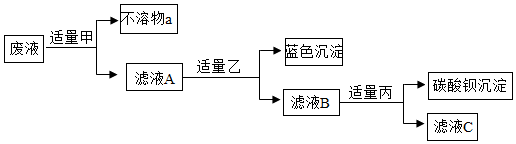
已知滤液B中只含有一种溶质,则下列说法不正确的是( )
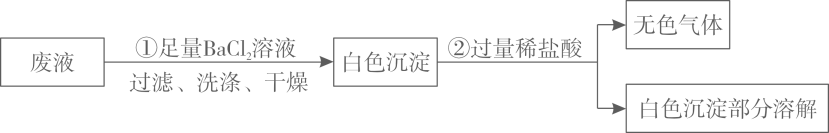
根据以上实验现象分析,可以得出原废液中( )
①取少量固体于试管中,加适量蒸馏水,固体完全溶解成无色透明溶液。
②取少量上述溶液,加过量稀硫酸,有气泡产生。
③取②中所得溶液少量,滴加BaCl2溶液,产生白色沉淀。
分析上述现象,对原固体组成的推断正确的是( )
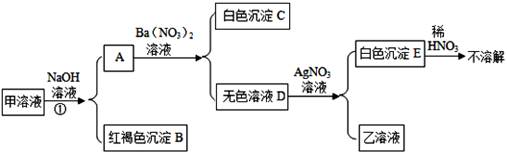

①取少量固体于试管中,加适量蒸馏水,固体完全溶解成无色透明溶液。
②取少量上述溶液,加过量稀硫酸,有气泡产生。
③取②中所得溶液少量,滴加BaCl2 溶液,产生白色沉淀。分析上述现象,对原固体组成的推断正确的是( )
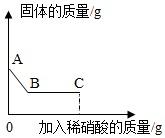
①取少量白色固体于烧杯中,向烧杯中加入足量水并不断搅拌,固体部分溶解;
②继续向烧杯中逐滴加入足量稀硝酸并不断搅拌,此时固体质量变化如图。
下列说法正确的是( )
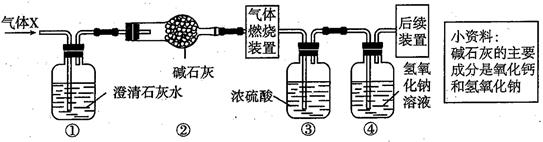
①除去二氧化碳中混有的少量氧气,可以通入一氧化碳后点燃,将氧气转化为二氧化碳;
②实验室用6%的氯化钠溶液配制3%的氯化钠溶液,量取6%的氯化钠溶液时俯视读数,若其他操作均正确,则所配溶液中溶质的质量分数大于3%;
③某固体可能由氯化钠、硫酸钠、氯化钡、氯化镁、硫酸钾中的一种或几种组成,取少量该固体,加入足量的稀氢氧化钠溶液,产生白色沉淀,过滤,向沉淀中加入足量稀硝酸,沉淀部分溶解,则该固体的组成有5种情况;
④某碳酸钠溶液中可能含有另一种溶质,取一定量该溶液,逐滴滴加稀盐酸,产生气体的体积与加入稀盐酸的体积关系如图所示,则该碳酸钠溶液中一定含有氢氧化钠。

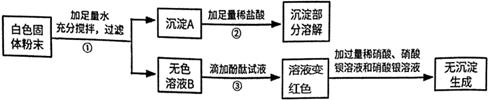

根据上述实验现象判断:
白色固体中一定不含,一定含有,可能含有;
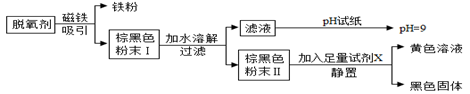
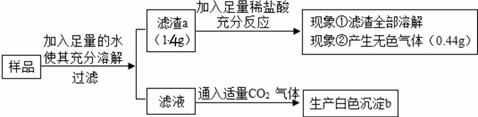
步骤Ⅰ:取少量固体样品置于烧杯中先加足量水溶解,再加入足量的BaCl2溶液,有白色沉淀产生。
步骤Ⅱ:继续向烧杯中滴加稀盐酸并不断搅拌,烧杯内固体质量随加入稀盐酸质量的变化如图所示,请回答下列问题:

|
实验内容 |
观察到的现象 |
|
A+B |
有气泡产生 |
|
A+C |
有白色沉淀生成 |
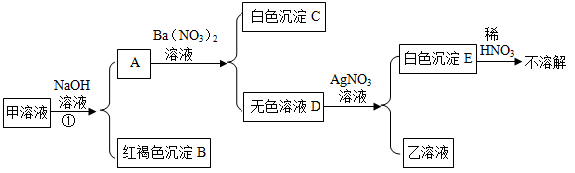
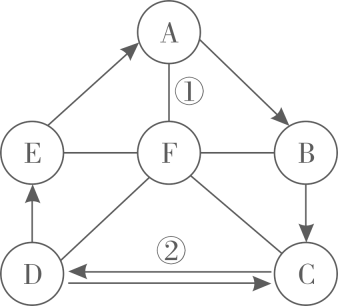
将三瓶无色溶液任意编号为A、B、C,各取少量进行实验,得到相关的实验记录(如表)。
请你判断B是溶液(填化学式);写出A与C反应的化学方程式。
①用三支试管分别取少量三种无色溶液;②滴加少量的;③观察现象;④得出结论。
Fe2O3+3H2 2Fe+3H2O。
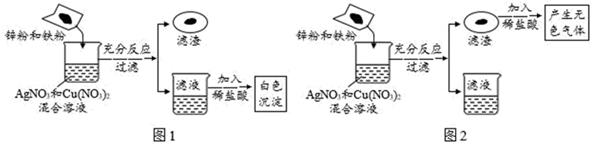
①滤液中一定含有的金属离子为(填离子符号)
②写出一个产生滤渣的反应的化学方程式.
①滤渣中一定含有(填化学式,下同)
②滤液中可能含有.
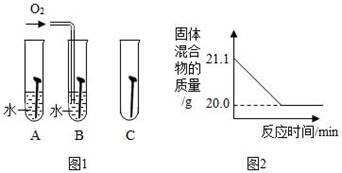
①下列不属于铁合金的是(选填字母)。
A.Fe(OH)3 B. 生铁 C. 不锈钢
②图1是探究铁钉在不同条件下发生生锈的实验,其中铁锈蚀最快的是(选填字母)。
在Fe2O3中,氧元素的质量分数为 。
①由图可知:生成CO2气体的质量为 g。
②计算反应后固体混合物中FeO的质量分数 (请根据化学方程式写出完整的计算步骤)
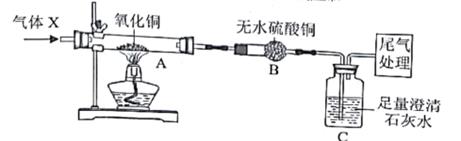
②铜和氧化亚铜均为不溶于水的红色固体;③Cu2O+H2SO4=CuSO4+Cu+H2O
小乐为了探究反应所得红色固体的成分,进行了如下实验: .
|
实验操作 |
|||
|
步骤一 |
取20g红色固体于烧杯中,加入足量稀硫酸 |
|
红色固体可能是氧化亚铜,也可能是铜和氧化亚铜 |
|
步骤二 |
将步骤一反应所得的混合物经过滤、洗涤、干燥并称量剩余红色固体质量 |
剩余红色固体质量为12g |
20g红色固体中,铜和氧化亚铜的质量比为 |
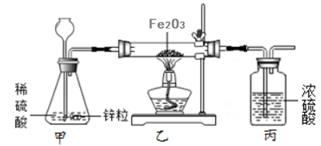
实验过程:连接好装置并检查装置的气密性,装入药品。打开活塞,让A中产生的气体依次通过B、C,待气体充满集气瓶后,用坩埚钳夹住8~ 10cm长的用砂纸打磨干净的镁条,将镁条点燃后迅速插入到正不断通入CO2的集带孔塑料板气瓶中,待剧烈反应平息后,关闭活塞,即可看到集气瓶内壁和底部有白色固体和黑色固体物质出现。
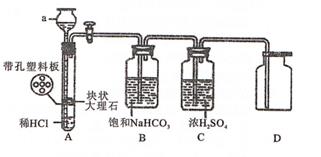
查阅资料:
①饱和NaHCO3溶液可以吸收HCl而不吸收CO2;②MgO、Mg(OH)2、MgCO3均为白色固体。
猜想Ⅰ:白色固体物质是MgO
猜想Ⅱ:白色固体物质是Mg(OH)2
猜想Ⅲ:白色固体物质是MgCO3
①上述猜想中,你认为不合理的猜想是(选填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
②乙同学取D中生成的白色固体于试管中,向其中加入足量的稀硫酸,固体溶解,无气泡产生。则镁在D中发生反应的化学方程式是 。
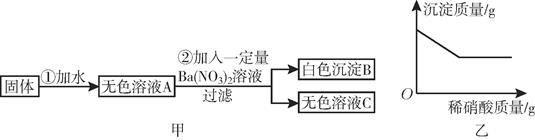
【组成确定】为确定四氧化三铁中可能含有的杂质,同学们进行了下列实验探究。
【查阅资料】
资料一:难溶性碱受热时能分解产生金属氧化物和水(反应中各种元素的化合价不变);
资料二:Fe2O3和CO反应是随温度升高而逐步进行的,先生成Fe3O4 , 再生成FeO(黑色),最后生成Fe;
【提出猜想】Fe3O4中可能含有的杂质是Fe2O3和FeO中的一种或两种。
【实验设计】同学们称取了23.28g该Fe3O4样品进行了下列实验(图2):
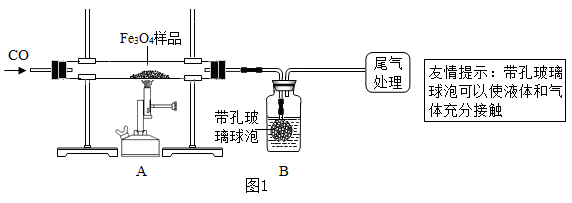
【实验分析】因探究思路不同,兴趣小组分成甲、乙两小组。
甲组:
①澄清石灰水 ②氢氧化钠浓溶液 ③稀盐酸 ④水
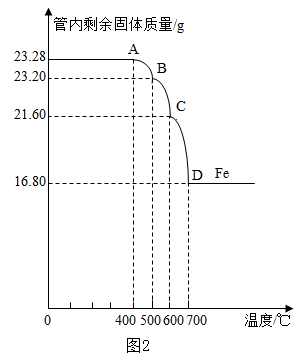
| 装置 | 反应前 | 反应后 |
| A | 试管的质量36.2 克 氧化铜和炭粉混合物的质量20.0克 |
试管和固体物质的质量54.8 克 |
| B | 反应后瓶内液体比反应前增重1.1 克 | |
分析数据发现,反应中消耗碳和氧元素的质量大于生成二氧化碳的质量.下列4项中跟这一结果有关的有哪几项? (填编号)
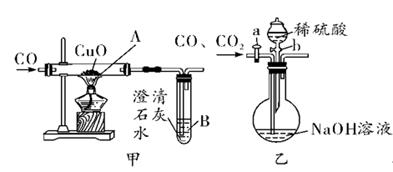
【查阅资料】:①氧化铜经一氧化碳还原不仅能生成铜,还可能生成中间产物氧化亚铜(Cu2O);②Cu2O是不溶于水的红色固体,能与酸发生反应,生成Cu2+和Cu。
【提出猜想】:氧化铜经一氧化碳还原所得到的红色固体中除Cu外还可能含有Cu2O。
【进行实验】:小明设计了一个最简单的实验方案:
|
实验步骤 |
取少量该红色固体放入盛有的试管中,振荡 |
|
实验现象及结论 |
|