B .
B .  C .
C .  D .
D . 
“疯狂”的星球

金星是太阳系中八大行星之一,中国古代称之为长庚、启明、太白金星。金星地表大气压约是地球的90倍,大气成分主要由二氧化碳组成,约占96%,因此它的地表具有强烈的温室效应,在近赤道的低地,温度可高达500℃。
在高度50至70公里的金星上空,悬浮着浓密的厚云,把大气分割为上下两层。你知道吗?地球云层的主要成分是水(水的液滴),而金星云层的主要成分是硫酸(硫酸的液滴),其中还掺杂着硫的粒子,所以呈现黄色。H2SO4的生成主要源于太阳光中波长短于160nm的紫外光对CO2的光解,使其变为CO和原子氧,原子氧非常活泼,能与SO2反应变为SO3 , SO3与水反应变为H2SO4 , 在金星,下的雨真是名副其实的酸雨。金星里,H2SO4的形成过程是不断循环的,H2SO4从大气较高较冷的区域降至较低较热的区域,当温度达到300℃时,H2SO4开始分解为SO3和水,SO3再分解为SO2和原子氧,原子氧接着与CO反应变为CO2。SO2与水会上升到上层,重新反应又释放出H2SO4。
依据文章内容,回答下列问题。
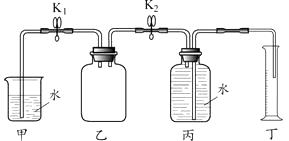
步骤如下:
① 关闭K2、打开K1 , 检查乙装置气密性,向乙中加入锌粒和稀硫酸,塞紧胶塞。
② 待气泡连续均匀产生,关闭K1、打开K2 , 并开始计时。
③ 待丁中收集到10 mL水,结束计时。
④ 换不同溶质质量分数、不同体积的硫酸,与质量相同的同一种锌粒重复实验。
每次实验的数据记录如下表:
实验 | 1 | 2 | 3 | 4 | 5 | 6 |
硫酸用量/mL | 10 | 20 | 40 | 10 | 20 | 40 |
硫酸的溶质质量分数/% | 10 | 10 | 10 | 20 | 20 | 20 |
收集所用时间/s | 106 | 102 | 97 | 45 | 41 | 40 |
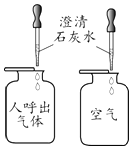
【查阅资料】通常情况下:二氧化碳在饱和碳酸氢钠溶液中
不溶;1体积水约能溶解1体积二氧化碳。
【进行实验】实验小组设计了如下图实验装置进行探究。
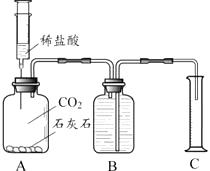

A中发生反应的化学方程式为。