选择题
| 选项 | 实验操作及现象 | 结论 |
| | 常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现象 | 稀硝酸的氧化性比浓硝酸强 |
| | 取一定量 | 此样品中含有 |
| | 将银和 |
|
| | 向溴水中加入苯,振荡后静置,水层颜色变浅 | 溴与苯发生了加成反应 |
- A、 A
- B、 B
- C、 C
- D、 D
- A、 自然固氮、人工固氮都是将
转化为
- B、 侯氏制碱法以
、
、
、
为原料制备
和
- C、 工业上通过
催化氧化等反应过程生产
- D、 多种形态的氮及其化合物间的转化形成了自然界的“氮循环”

- A、 甲是空气中体积分数最大的成分
- B、 乙是引起温室效应的气体之一
- C、 反应(Ⅰ)在常温下容易发生
- D、 反应(Ⅱ)中NO是氧化剂

- A、
分子的共价键是
键,
分子的共价键是
键
- B、 燃烧生成的
气体与空气中的水蒸气结合呈雾状
- C、 停止反应后,用蘸有浓氨水的玻璃棒靠近集气瓶口产生白烟
- D、 可通过原电池将
与
反应的化学能转化为电能
- A、 工业上通过电解六水合氯化镁制取金属镁
- B、 接触法制硫酸时,煅烧黄铁矿以得到三氧化硫
- C、 浓硝酸与铁在常温下不反应,所以可用铁质容器贮运浓硝酸
- D、 “洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用
| 选项 | 性质 | 解释 |
| A | 比 | |
| B | 熔点高于 | |
| C | 能与 | |
| D | 氨水中存在 | |
- A、 A
- B、 B
- C、 C
- D、 D
- A、 向NaHSO3溶液中滴加氢硫酸,产生淡黄色沉淀,证明HSO
具有氧化性
- B、 向酸性KMnO4溶液中加入Fe3O4粉末,紫色褪去,证明Fe3O4中含Fe(Ⅱ)
- C、 向浓HNO3中插入红热的炭,产生红棕色气体,证明炭可与浓HNO3反应生成NO2
- D、 向NaClO溶液中滴加酚酞试剂,先变红后褪色,证明NaClO在溶液中发生了水解反应
| 选项 | 生产活动 | 化学原理 |
| A | 用聚乙烯塑料制作食品保鲜膜 | 聚乙烯燃烧生成 |
| B | 利用海水制取溴和镁单质 | |
| C | 利用氢氟酸刻蚀石英制作艺术品 | 氢氟酸可与 |
| D | 公园的钢铁护栏涂刷多彩防锈漆 | 钢铁与潮湿空气隔绝可防止腐蚀 |
- A、 A
- B、 B
- C、 C
- D、 D
| 选项 | 劳动项目 | 化学知识 |
| A | 社区服务:用84消毒液对图书馆桌椅消毒 | 含氯消毒剂具有氧化性 |
| B | 学农活动:用厨余垃圾制肥料 | 厨余垃圾含 |
| C | 家务劳动:用白醋清洗水壶中的水垢 | 乙酸可由乙醇氧化制备 |
| D | 自主探究:以油脂为原料制肥皂 | 油脂可发生皂化反应 |
- A、 A
- B、 B
- C、 C
- D、 D
| 选项 | 操作或做法 | 目的 |
| A | 将铜丝插入浓硝酸中 | 制备 |
| B | 将密闭烧瓶中的 | 探究温度对平衡移动的影响 |
| C | 将溴水滴入 | 萃取溶液中生成的碘 |
| D | 实验结束,将剩余 | 节约试剂 |
- A、 A
- B、 B
- C、 C
- D、 D
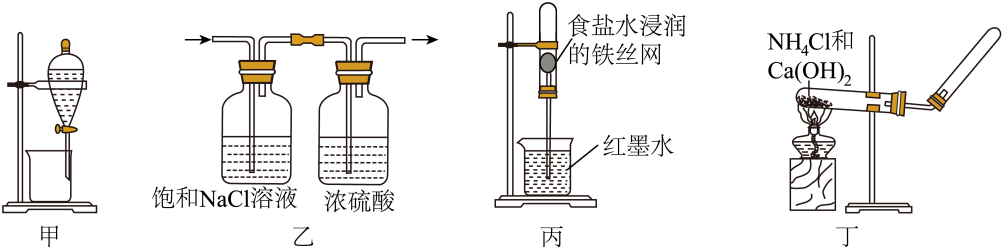
| 气体 | 方法 | |
| A | 氨气 | 加热氯化铵固体 |
| B | 二氧化氮 | 将铝片加到冷浓硝酸中 |
| C | 硫化氢 | 向硫化钠固体滴加浓硫酸 |
| D | 氧气 | 加热氯酸钾和二氧化锰的混合物 |
- A、 A
- B、 B
- C、 C
- D、 D
| 实验目的 | 实验设计 | |
| A | 检验溶液中 | 取少量待测液,滴加 |
| B | 净化实验室制备的 | 气体依次通过盛有饱和 |
| C | 测定 | 将待测液滴在湿润的pH试纸上,与标准比色卡对照 |
| D | 工业酒精制备无水乙醇 | 工业酒精中加生石灰,蒸馏 |
- A、 A
- B、 B
- C、 C
- D、 D

下列说法错误的是( )
- A、 物质X常选用生石灰
- B、 工业上常用电解熔融
制备金属镁
- C、 “氯化”过程中发生的反应为
- D、 “煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水
- A、 NO2和SO2均为红棕色且有刺激性气味的气体,是酸雨的主要成因
- B、 汽车尾气中的主要大气污染物为NO、SO2和PM2.5
- C、 植物直接吸收利用空气中的NO和NO2作为肥料,实现氮的固定
- D、 工业废气中的SO2可采用石灰法进行脱除
- A、 浓H2SO4具有强吸水性,能吸收糖类化合物中的水分并使其炭化
- B、 NaClO、KClO3等氯的含氧酸盐的氧化性会随溶液的pH减小而增强
- C、 加热NaI与浓H3PO4混合物可制备HI,说明H3PO4比HI酸性强
- D、 浓HNO3和稀HNO3与Cu反应的还原产物分别为NO2和NO,故稀HNO3氧化性更强
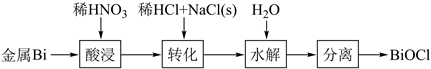
下列说法错误的是( )
- A、 酸浸工序中分次加入稀HNO3可降低反应剧烈程度
- B、 转化工序中加入稀HCl可抑制生成BiONO3
- C、 水解工序中加入少量CH3COONa(s)可提高Bi3+水解程度
- D、 水解工序中加入少量NH4NO3(s)有利于BiOCl的生成
- A、 用碳酸钠溶液处理水垢中的硫酸钙: CO32- +CaSO4 =CaCO3 + SO42-
- B、 过量铁粉加入稀硝酸中:Fe + 4H+ + NO3- = Fe3+ +NO↑ +2H2O
- C、 硫酸铝溶液中滴如少量氢氧化钾溶液: Al3+ +4 OH- =AlO2- + 2H2O
- D、 氯化铜溶液中通入硫化氢: Cu2+ + S2- =CuS ↓
- A、 某些胶态金属氧化物分散于玻璃中可制造有色玻璃
- B、 通常以海水提取粗食盐后的母液为原料制取溴
- C、 生物炼铜中通常利用某些细菌把不溶性的硫化铜转化为可溶性铜盐
- D、 工业制备硝酸的主要设备为沸腾炉、接触室和吸收塔
非选择题
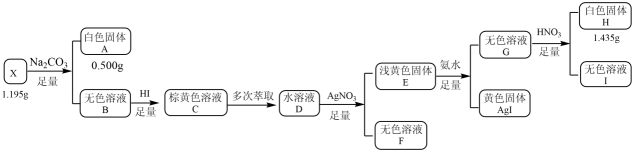
已知:白色固体A用溶解后,多余的酸用
恰好中和,请回答:
资料:i.Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、(绿色)、
(紫色)。
ii.浓碱条件下,可被OH-还原为
。
iii.Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)

序号 | 物质a | C中实验现象 | |
通入Cl2前 | 通入Cl2后 | ||
I | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
II | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
III | 40%NaOH 溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |

回答问题:
①称取 ,配成
溶液,转移至恒压滴液漏斗中。
②向三颈烧瓶中加入 溶液。
③持续磁力搅拌,将 溶液以
的速度全部滴入三颈烧瓶中,100℃下回流3h。
④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在 干燥。
⑤管式炉内焙烧2h,得产品3.24g。
部分装置如图:

回答下列问题:
已知:①
②沸点: 为-6℃,
为-34℃,
为-152℃。
③ 易水解,能与
反应。
某研究小组用 和
在如图所示装置中制备
,并分离回收未反应的原料。

回答问题: