选择题
试题详情
下列有关电极方程式或离子方程式错误的是
- A、 碱性锌锰电池的正极反应:MnO2+H2O+e-=MnO(OH)+OH-
- B、 铅酸蓄电池充电时的阳极反应:Pb2++2H2O-2e-=PbO2+4H+
- C、 K3[Fe(CN)6]溶液滴入FeCl2溶液中:K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓
- D、 TiCl4加入水中:TiCl4+(x+2)H2O=TiO2·xH2O↓+4H++4Cl-
试题详情
油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄 褪色的主要原因是发生了以下两种化学反应:
褪色的主要原因是发生了以下两种化学反应:

下列说法正确的是
- A、
和
的空间结构都是正四面体形
- B、 反应Ⅰ和Ⅱ中,元素
和S都被氧化
- C、 反应Ⅰ和Ⅱ中,参加反应的
:Ⅰ<Ⅱ
- D、 反应Ⅰ和Ⅱ中,氧化
转移的电子数之比为3∶7
试题详情
葡萄糖酸钙是一种重要的补钙剂,工业上以葡萄糖、碳酸钙为原料,在溴化钠溶液中采用间接电氧化反应制备葡萄糖酸钙,其阳极区反应过程如下:

下列说法错误的是
- A、 溴化钠起催化和导电作用
- B、 每生成
葡萄糖酸钙,理论上电路中转移了
电子
- C、 葡萄糖酸能通过分子内反应生成含有六元环状结构的产物
- D、 葡萄糖能发生氧化、还原、取代、加成和消去反应
试题详情
一定条件下,酸性 溶液与
溶液与 发生反应,
发生反应, (Ⅱ)起催化作用,过程中不同价态含
(Ⅱ)起催化作用,过程中不同价态含 粒子的浓度随时间变化如下图所示。下列说法正确的是
粒子的浓度随时间变化如下图所示。下列说法正确的是

- A、
(Ⅲ)不能氧化
- B、 随着反应物浓度的减小,反应速率逐渐减小
- C、 该条件下,
(Ⅱ)和
(Ⅶ)不能大量共存
- D、 总反应为:
试题详情
科技是第一生产力,我国科学家在诸多领域取得新突破,下列说法错误的是
- A、 利用CO2合成了脂肪酸:实现了无机小分子向有机高分子的转变
- B、 发现了月壤中的“嫦娥石[(Ca8Y)Fe(PO4)7]”:其成分属于无机盐
- C、 研制了高效率钙钛矿太阳能电池,其能量转化形式:太阳能→电能
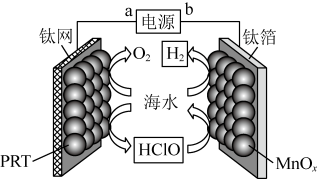
- D、 革新了海水原位电解制氢工艺:其关键材料多孔聚四氟乙烯耐腐蚀
试题详情
下列化学事实不符合“事物的双方既相互对立又相互统一”的哲学观点的是
- A、 石灰乳中存在沉淀溶解平衡
- B、 氯气与强碱反应时既是氧化剂又是还原剂
- C、 铜锌原电池工作时,正极和负极同时发生反应
- D、 Li、Na、K的金属性随其核外电子层数增多而增强
试题详情
工业制备高纯硅的主要过程如下:
石英砂粗硅
高纯硅
下列说法错误的是
- A、 制备粗硅的反应方程式为
- B、 1molSi含Si-Si键的数目约为
- C、 原料气HCl和
应充分去除水和氧气
- D、 生成
的反应为熵减过程
试题详情
我国科学家设计如图所示的电解池,实现了海水直接制备氢气技术的绿色化。该装置工作时阳极无 生成且KOH溶液的浓度不变,电解生成氢气的速率为
生成且KOH溶液的浓度不变,电解生成氢气的速率为 。下列说法错误的是
。下列说法错误的是
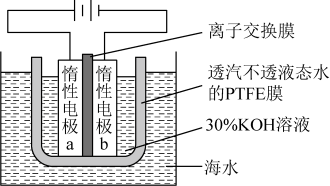
- A、 b电极反应式为
- B、 离子交换膜为阴离子交换膜
- C、 电解时海水中动能高的水分子可穿过PTFE膜
- D、 海水为电解池补水的速率为
试题详情
室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应: S8+e-→
S8+e-→ S
S ,
,  S
S +e-→S
+e-→S , 2Na++
, 2Na++ S
S +2(1-
+2(1- )e-→Na2Sx
)e-→Na2Sx
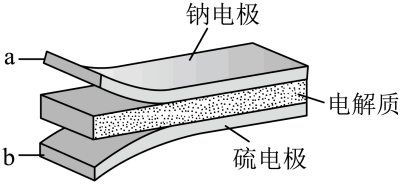
下列叙述错误的是
- A、 充电时Na+从钠电极向硫电极迁移
- B、 放电时外电路电子流动的方向是a→b
- C、 放电时正极反应为:2Na++
S8+2e-→Na2Sx
- D、 炭化纤维素纸的作用是增强硫电极导电性能
试题详情
一些化学试剂久置后易发生化学变化。下列化学方程式可正确解释相应变化的是
A | 硫酸亚铁溶液出现棕黄色沉淀 | |
B | 硫化钠溶液出现浑浊颜色变深 | |
C | 溴水颜色逐渐褪去 | |
D | 胆矾表面出现白色粉末 |
- A、 A
- B、 B
- C、 C
- D、 D
试题详情
“肼合成酶”以其中的 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼(
转化为肼( ),其反应历程如下所示。
),其反应历程如下所示。
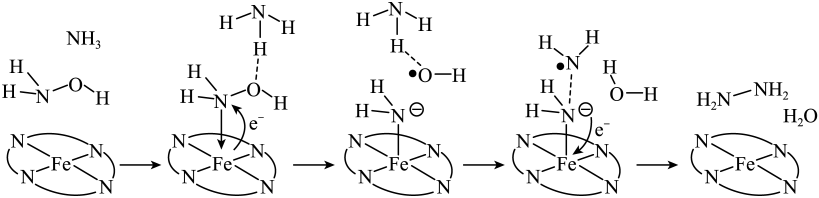
下列说法错误的是
- A、
、
和
均为极性分子
- B、 反应涉及
、
键断裂和
键生成
- C、 催化中心的
被氧化为
, 后又被还原为
- D、 将
替换为
, 反应可得
试题详情
根据实验操作及现象,下列结论中正确的是
| 选项 | 实验操作及现象 | 结论 |
| | 常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现象 | 稀硝酸的氧化性比浓硝酸强 |
| | 取一定量 | 此样品中含有 |
| | 将银和 |
|
| | 向溴水中加入苯,振荡后静置,水层颜色变浅 | 溴与苯发生了加成反应 |
- A、 A
- B、 B
- C、 C
- D、 D
试题详情
用可再生能源电还原 时,采用高浓度的
时,采用高浓度的 抑制酸性电解液中的析氢反应来提高多碳产物(乙烯、乙醇等)的生成率,装置如下图所示。下列说法正确的是
抑制酸性电解液中的析氢反应来提高多碳产物(乙烯、乙醇等)的生成率,装置如下图所示。下列说法正确的是
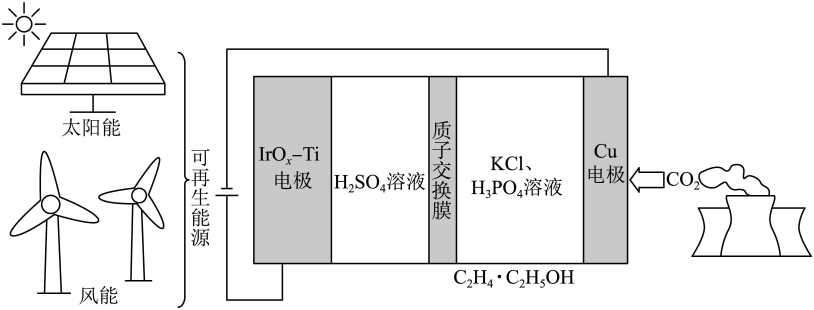
- A、 析氢反应发生在
电极上
- B、
从
电极迁移到
电极
- C、 阴极发生的反应有:
- D、 每转移
电子,阳极生成
气体(标准状况)
试题详情
在熔融盐体系中,通过电解 和
和 获得电池材料
获得电池材料 , 电解装置如图,下列说法正确的是
, 电解装置如图,下列说法正确的是
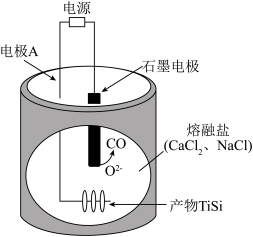
- A、 石墨电极为阴极,发生氧化反应
- B、 电极A的电极反应:
- C、 该体系中,石墨优先于
参与反应
- D、 电解时,阳离子向石墨电极移动
非选择题
试题详情
聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。
试题详情
超纯 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯
是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,工业上以粗镓为原料,制备超纯
方面取得了显著成果,工业上以粗镓为原料,制备超纯 的工艺流程如下:
的工艺流程如下:

已知:①金属的化学性质和
相似,
的熔点为
;
②(乙醚)和
(三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:
| 物质 | | | | |
| 沸点/ | 55.7 | 34.6 | 42.4 | 365.8 |
回答下列问题:
试题详情
硫酸工业在国民经济中占有重要地位。
试题详情
某工厂采用如下工艺处理镍钴矿硫酸浸取液含( 和
和 )。实现镍、钴、镁元素的回收。
)。实现镍、钴、镁元素的回收。

已知:
| 物质 | | | | |
| | | | | |
回答下列问题:
试题详情  是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下:
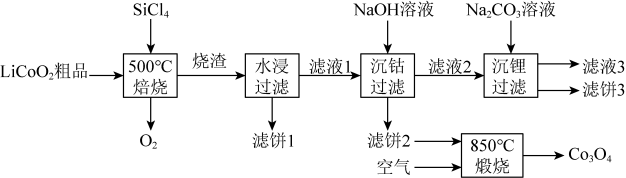
回答下列问题:
试题详情
学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
试题详情
纳米碗 是一种奇特的碗状共轭体系。高温条件下,
是一种奇特的碗状共轭体系。高温条件下, 可以由
可以由 分子经过连续5步氢抽提和闭环脱氢反应生成。
分子经过连续5步氢抽提和闭环脱氢反应生成。 的反应机理和能量变化如下:
的反应机理和能量变化如下:
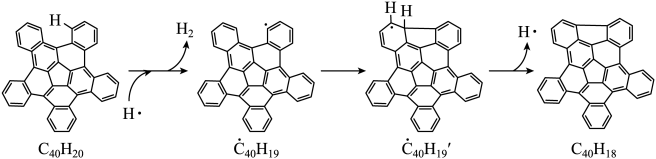
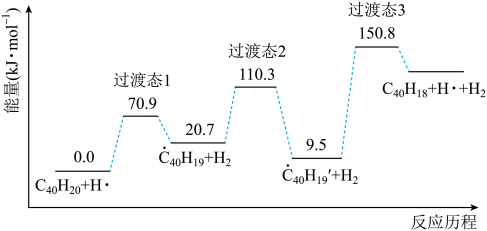
回答下列问题:
试题详情
LiMn2O4作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO3 , 含有少量Si、Fe、Ni、Al等元素)制备LiMn2O4的流程如下:
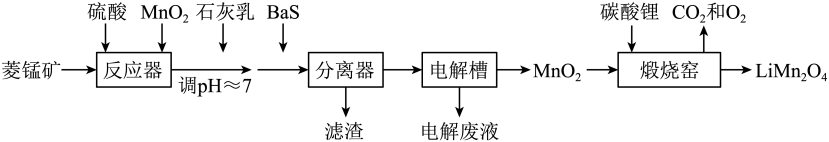
已知:Ksp[Fe(OH)3]=2.8×10-39 , Ksp[Al(OH)3]=1.3×10-33 , Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
试题详情
硫酸亚铁在工农业生产中有许多用途,如可用作农药防治小麦黑穗病,制造磁性氧化铁、铁催化剂等。回答下列问题:
试题详情
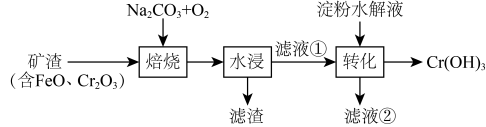
铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:

已知:最高价铬酸根在酸性介质中以存在,在碱性介质中以
存在。
回答下列问题:
试题详情  是一种压电材料。以
是一种压电材料。以 为原料,采用下列路线可制备粉状
为原料,采用下列路线可制备粉状 。
。
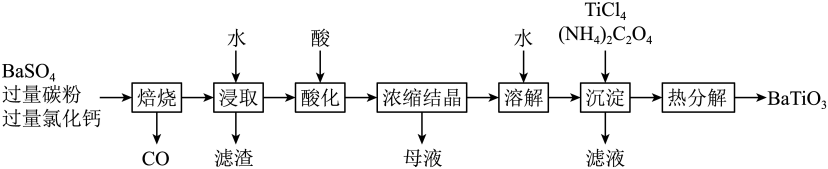
回答下列问题:
试题详情
甲烷选择性氧化制备甲醇是一种原子利用率高的方法。回答下列问题:
试题详情
“碳达峰·碳中和”是我国社会发展重大战略之一, 还原
还原 是实现“双碳”经济的有效途径之一,相关的主要反应有:
是实现“双碳”经济的有效途径之一,相关的主要反应有:
Ⅰ:
Ⅱ:
请回答: