选择题
实验方案 | 现象 | 结论 | |
A | 往 | 短时间内无明显现象 |
|
B | 往 | 溶液先变成血红色后无明显变化 |
|
C | 将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加 | 溶液呈浅绿色 | 食品脱氧剂样品中没有 |
D | 向沸水中逐滴加5~6滴饱和 | 溶液先变成红褐色再析出沉淀 |
|
- A、 A
- B、 B
- C、 C
- D、 D
- A、 鎏金工艺利用了汞的挥发性
- B、 鎏金工艺中金发生了化学反应
- C、 鎏金工艺的原理可用于金的富集
- D、 用电化学方法也可实现铜上覆金
- A、 与稀硫酸反应: Cr2O3+ 3H2SO4 = Cr2(SO4)3+ 3H2O
- B、 与NaOH溶液反应: Cr2O3+ 4OH- = 2
+2H2O
- C、 碱性条件下被H2O2氧化为Cr(+6): Cr2O3+ 3H2O2+ 4OH- =2
+ 5H2O
- D、 由于金属性铝强于铬,且铬的熔点较高,故可用铝热法还原Cr2O3制取金属铬
- A、 碳纳米管属于胶体,具有较高强度
- B、 淀粉、纤维素、脂肪、蛋白质都是天然高分子化合物
- C、 除去锅炉中的水垢时,可先用碳酸钠溶液处理,使水垢蓬松,再加入酸去除
- D、 碳酸钡可用于肠胃X射线造影检查

下列说法正确的是( )
- A、 步骤①操作中,生成的气体可用
溶液吸收
- B、 检验滤液1中是否含有
,可以选用
和新制的氯水
- C、 步骤③和④操作中,均采用蒸发结晶方式从溶液中获得溶质
- D、 滤渣2成分是
- A、 “凡播种先以稻麦稿包浸数日俟其生芽撒于田中生出寸许其名曰秧。”。其中“稻麦稿”的主要成分纤维素。
- B、 “水火既济而土合······后世方土效灵人工表异陶成雅器有素肌、玉骨之象焉”以上所述的“陶成雅器”的主要原料是黏土、石灰石
- C、 “凡火药,硫为纯阳,硝为纯阴,此乾坤幻出神物也”,“硝”指的是硝酸钾。
- D、 “凡铸镜模用灰沙铜用锡和”该法所制铜镜主要成分为青铜。
- A、 分子筛常用于分离、提纯气体混合物,但不能用于液体混合物分离
- B、
可用作医疗上检查肠胃的钡餐,还可用作白色颜料
- C、 光照下,
在空气中与碳氢化合物发生作用,可产生光化学烟雾
- D、 铁的化合物应用广泛,
常用作净水剂
- A、
、
、
均可以由相应单质直接化合生成
- B、 浓盐酸、浓硝酸、浓硫酸均可用铝罐车运输
- C、 等质量的铜分别与足量的浓硝酸和稀硝酸充分反应,转移的电子数相等
- D、 将氯气通入紫色石蕊溶液中,溶液先变红后褪色,说明氯气具有漂白性和酸性

- A、 根据反应③可知氧化性:Fe3+>H2O2
- B、 向X溶液中滴入K3[Fe(CN)6]溶液,生成蓝色沉淀
- C、 反应③中稀硫酸仅表现酸性
- D、 反应①的离子方程式为Cu+H2O2+2H+=Cu2++2H2O

- A、 “溶解”过程中发生的反应有2Cu+O2+4H+=2Cu2++2H2O
- B、 “溶解”操作中的空气可以用双氧水代替
- C、 “调节pH”过程中NaOH溶液的作用是使Cu2+转化为Cu(OH)2
- D、 “过滤II”所得滤渣只需洗涤,无需干燥

下列说法正确的是( )
- A、 PbO在NaOH溶液中的溶解是放热反应
- B、 碱浸1适宜用高浓度的NaOH溶液
- C、 降低NaOH溶液的浓度有利于PbO溶解
- D、 M点溶液中存在

下列说法错误的是( )
- A、 ①中生成了
:
- B、 操作
是过滤,以除去难溶于
溶液的杂质
- C、 ②③中加入稀硫酸的作用均是除去杂质
- D、 由④可知,室温下明矾的溶解度小于
和
的溶解度
| 实验操作 | 实验现象 | ||
| 金属为铜 | 金属为锌 | 金属为铝 | |
| 点燃 | 不燃烧 | 燃烧 | 燃烧 |
| 通入 | 褪色 | 褪色 | 褪色 |
| 通入 | 无明显变化 | 无明显变化 | 出现黑色沉淀 |
| 通入品红溶液 | 褪色 | 褪色 | 不褪色 |
已知: (CuS为黑色固体);
可燃
下列说法错误的是( )
- A、 加入铜片的实验中,使
酸性溶液褪色的气体是
- B、 加入铝片的实验中,燃烧现象能证明生成气体中一定含
- C、 加入锌片的实验中,生成的气体一定是混合气体
- D、 金属与浓硫酸反应的还原产物与金属活动性强弱有关
- A、 N2(g)
NO(g)
HNO3(aq)
- B、 Al2O3(s)
Al(s)
NaAlO2(aq)
- C、 BaCl2(aq)
BaCO3(s)
BaSO4(s)
- D、 MgCl2·6H2O(s)
MgCl2(s)
Mg(s)
- A、 粗硅
SiCl4
Si
- B、 Mg(OH)2
MgCl2(aq)
Mg
- C、 Fe2O3
FeCl3(aq)
无水FeCl3
- D、 AgNO3(aq)
[Ag(NH3)2]OH(aq)
Ag
非选择题
 已知:25℃时,
已知:25℃时, 的
,
;
;
;该工艺中,
时,溶液中
元素以
的形态存在。
 已知:苯甲酸是一元弱酸,白色片状晶体,常温下微溶于水,温度升高,溶解度增大。
已知:苯甲酸是一元弱酸,白色片状晶体,常温下微溶于水,温度升高,溶解度增大。
回答下列问题:
 其中:X由三种短周期元素组成,且阴、阳离子个数比为2:1;金属互化物——全部由金属元素组成的化合物。
其中:X由三种短周期元素组成,且阴、阳离子个数比为2:1;金属互化物——全部由金属元素组成的化合物。
请回答:

回答下列问题:


已知:LiOH易溶于水,Li2CO3微溶于水。回答下列问题:

已知:H2S的电离常数K1=1.3×10-7 , K2=7.1×10-15;Ksp[CuS]=6.0×10-36;Ksp[Ni(OH)2]=1.0×10-15.6
回答下列问题:

完成下列填空:

回答下列问题:

回答下列问题:
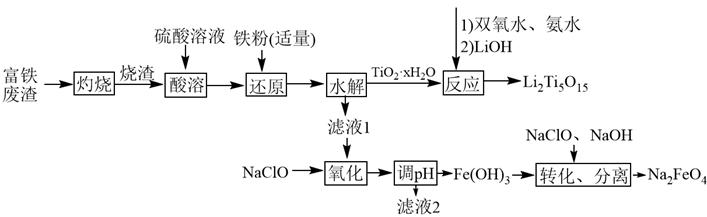
已知: 、
、
,溶液中离子浓度
时认为该离子沉淀完全。回答下列问题:
实验记录如下:
| | 实验 | 方案和现象 |
| ⅰ | 加入1mL蒸馏水,再滴加1滴品红溶液,品红溶液较快褪色 | |
| ⅱ | 加入少量Ag2O固体,产生白色沉淀a。再加入1mL蒸馏水和 1滴品红溶液,品红溶液褪色比i快 | |
| ⅲ | 加入1mL较浓AgNO3溶液,产生白色沉淀b。再滴加1滴品红溶液,品红溶液褪色比i慢 |
I.向粗锰粉中加入盐酸,控制溶液的pH约为5,测定离子的初始浓度。静置一段时间后锰粉仍略有剩余,过滤;
II.向I的滤液中加入一定量盐酸,再加入 溶液,充分反应后加入
固体调节溶液的pH约为5,过滤;
III.向II的滤液中通入 气体,待充分反应后加热一段时间,冷却后过滤;
IV.浓缩、结晶、过滤、洗涤、脱水得到无水MnCl2。
各步骤中对杂质离子的去除情况
| | | | |
| 初始浓度/mg·L–1 | 21.02 | 4.95 | 5.86 |
| 步骤I后/ mg·L–1 | 12.85 | 3.80 | 3.39 |
| 步骤II后/ mg·L–1 | 0.25 | 3.76 | 3.38 |
| 步骤III后/ mg·L–1 | 0.10(达标) | 3.19(未达标) | 0.12(达标) |
已知:金属活动性Mn>Fe>Ni>Pb