选择题
试题详情
一种用于发动机SCR系统的电解尿素( )混合装置(X、Y为石墨电极,隔膜仅阻止气体通过)如图,下列说法不正确的是
)混合装置(X、Y为石墨电极,隔膜仅阻止气体通过)如图,下列说法不正确的是
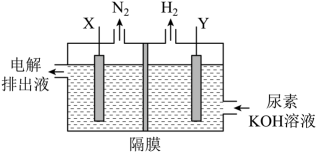
- A、 装置工作时,电子由Y极流入,X极流出
- B、 Y极发生还原反应
- C、 X极的电极反应式为
- D、 若用铅酸蓄电池为电源,理论上消耗49 g
时,此装置中有0.5mol
生成
试题详情
电极材料 制备的反应为
制备的反应为 , 下列说法正确的是
, 下列说法正确的是
- A、 生成0.1 mol
, 转移的电子数为0.1
- B、 还原产物为
和CO
- C、 标准状况下,生成20.16L CO时,被还原的
为0.1 mol
- D、 还原剂与氧化剂的物质的量之比为1∶6
试题详情
工业上利用含铅废渣(主要成分为 )制备碱式硫酸铅(
)制备碱式硫酸铅( )的简易流程如图所示。下列说法错误的是
)的简易流程如图所示。下列说法错误的是

- A、 “转化”过程生成的气体为
- B、 由流程可推测,
- C、 该工艺中滤液2可循环利用
- D、 该流程发生了氧化还原反应
试题详情
有机物Q的合成路线(反应条件和其他产物已经略去)如图所示,下列说法错误的是

- A、
最多能与
发生反应
- B、 在
的过程中,发生还原反应
- C、 Y能使溴水和酸性高锰酸钾溶液褪色,褪色原理不同
- D、 P和Q均易溶于水
试题详情
关于反应K2H3IO6+9HI=2KI+4I2+6H2O,下列说法正确的是
- A、 生成12.7g I2时,转移0.1mol电子
- B、 KI是还原产物
- C、 还原剂与氧化剂的物质的量之比为7:1
- D、 K2H3IO6发生氧化反应
试题详情
关于反应 , 下列说法正确的是
, 下列说法正确的是
- A、 该反应的氧化剂是硝酸钾
- B、 生成标准状况下2.24L
, 反应共转移1mol电子
- C、 氧化产物与还原产物的物质的量之比为3∶1
- D、 电负性:O>N>C>K
试题详情
化学性质类似 的盐酸羟胺(
的盐酸羟胺( )是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有(
)是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有( 、
、 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是

- A、 图1电池工作时,Pt电极是正极
- B、 图2中,A为
和
, B为
- C、 电极b接电源负极,处理1 mol
, 电路中转移5 mol
- D、 电池工作时,每消耗2.24 L NO(标准状况下),左室溶液质量增加3.3 g
试题详情  与砂糖混用为补血剂。合成
与砂糖混用为补血剂。合成 工艺流程如下:
工艺流程如下:

已知:“还原”工序中不生成S单质。下列说法错误的是
- A、 “焙烧”时,空气和
逆流可提高焙烧效率
- B、 “焙烧”过程中氧化剂和还原剂的物质的量之比为11∶4
- C、 “还原”工序中,反应的离子方程式为
- D、 “沉铁”时,
与
结合生成
, 促进了
的电离
试题详情
氮氧化物是大气污染物之一,如图为科研人员探究消除氮氧化物的反应机理,下列说法错误的是
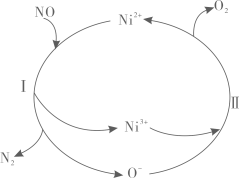
- A、 过程I中NO既作氧化剂又作还原剂
- B、 过程II中每生成1molO2时,转移电子的数目约为4×6.02×1023
- C、 过程中涉及的反应均为氧化还原反应
- D、 整个过程中Ni2+作催化剂
多选题
试题详情
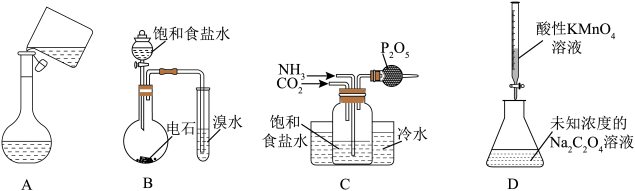
某同学用如图所示装置进行实验,预测现象与实际不相符的是

①中物质 | ②中物质 | 预期现象 | |
A | 乙醇 | 酸性KMnO4溶液 | 紫色溶液颜色变浅或退去 |
B | H2S溶液 | Na2SO3溶液 | 溶液变浑浊、产生气泡 |
C | H2O2溶液 | 淀粉KI溶液 | 溶液变蓝 |
D | 浓氨水 | AlCl3溶液 | 生成白色沉淀后又溶解 |
试题详情
电镀厂镀镍时,镍阳极板损耗后变成蜂窝状镍脱落成为镍阳极泥。我国镍资源短缺,因此利用镍阳极泥回收镍有着重要的意义。实验室中利用镍阳极泥(含有铁、铜等杂质)制取少量硫酸镍晶体( )的实验流程如图所示:
)的实验流程如图所示:

已知:“加热溶解”过程中加入少量浓硝酸起加快反应速率的作用。下列说法错误的( )
试题详情
一种以Pd―Cu为催化剂还原去除水体中 的机理如图a所示;其他条件相同,不同pH时,
的机理如图a所示;其他条件相同,不同pH时, 转化率和不同产物在总还原产物中所占的物质的量的百分比如图b所示。
转化率和不同产物在总还原产物中所占的物质的量的百分比如图b所示。

已知:溶液pH会影响Pd对的吸附,不影响对H的吸附。
下列说法正确的是( )
试题详情
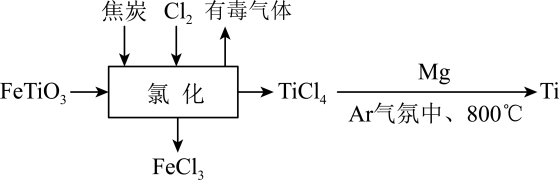
钛合金广泛应用于航空航海领域。钛铁矿(其中Ti为+4价)在高温下经氯化得到四氯化钛,再制取金属钛的流程如图所示。下列说法正确的是( )
试题详情
碘介导的醇歧化反应机理如下图所示(R一为烃基),下列说法正确的是( )

非选择题
试题详情
以银锰精矿 主要含
主要含 、
、 、
、 和氧化锰矿
和氧化锰矿 主要含
主要含 为原料联合提取银和锰的一种流程示意图如下。
为原料联合提取银和锰的一种流程示意图如下。
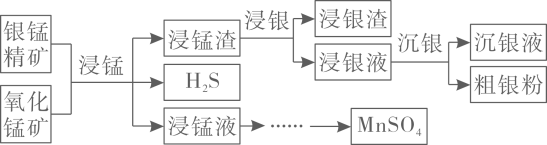
已知:酸性条件下,的氧化性强于
。
试题详情
资料显示, 可以将
可以将 氧化为
氧化为 。某小组同学设计实验探究
。某小组同学设计实验探究 被
被 氧化的产物及铜元素的价态。
氧化的产物及铜元素的价态。
已知:易溶于
溶液,发生反应
红棕色
;
和
氧化性几乎相同。
试题详情
某同学利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
回答下列问题:
试题详情
短周期的元素在自然界中比较常见,尤其是非金属元素及其化合物在社会生活中有着很重要的作用。
试题详情
某国产电动汽车推出的“刀片电池”具有强环境适应性,更安全可靠。“刀片电池”正极材料使用了磷酸亚铁锂(LiFePO4)。磷酸亚铁锂(LiFePO4)由Li2CO3、C6H12O6和FePO4在高温条件下制备。
试题详情
CS2是一种重要的化工原料。工业上可以利用硫(S8)与CH4为原料制备CS2 , S8受热分解成气态S2 , 发生反应2S2(g)+CH4(g) CS2(g)+2H2S(g),回答下列问题:
CS2(g)+2H2S(g),回答下列问题:
试题详情
含氯化合物有广泛的应用。
试题详情
金属钠及其化合物在人类生产、生活中起着重要作用。
试题详情
(NH4)2S2O8电化学循环氧化法可用于废水中苯酚的降解,示意图如图。

试题详情
实验小组模拟工业上回收“分银渣”中的银,过程如下:

I中反应:(杂质不反应)
试题详情
偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:(CH3)2NNH2(l)+2N2O4(l)=2CO2(g)+3N2(g)+4H2O(g)(I)
试题详情
某小组同学探究 与
与 溶液的反应,实验如下。
溶液的反应,实验如下。
资料:i.(黄色)
ii.呈绿色(酸性条件下不稳定)、低浓度
呈无色、MnS为肉色沉淀。
iii.
实验Ⅰ:
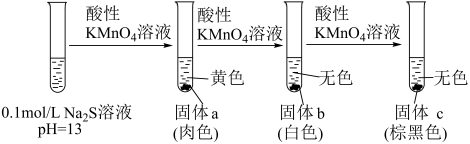
试题详情
某小组根据硫元素的化合价,预测SO2既有还原性又有氧化性,并设计实验进行探究。