选择题
试题详情  为阿伏加德罗常数的值,下列叙述正确的是( )
为阿伏加德罗常数的值,下列叙述正确的是( )
- A、 常温常压下,
金刚石含有4NA个共价键
- B、
的乙酸和盐酸混合溶液含0.1NA个
- C、 标准状态下,
含有的质子数为10NA
- D、 电解水生成
氢气,外电路通过1NA个电子
试题详情
反应 常被用于除去水中残余氯。
常被用于除去水中残余氯。 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
- A、
溶液中含有的
键数目为
- B、 25℃、101kPa时,
中氯原子的数目为
- C、
含有质子的数目为
- D、 通过上述反应除去
, 电子转移的数目为
试题详情
设NA为阿伏加德罗常数的值,下列叙述正确的是
- A、 1LpH=1的H2C2O4溶液中含有阳离子总数为0.2NA
- B、 12.0g二氧化硅晶体中含Si-O键的数目为0.4NA
- C、 常温下,1.6gO2与O3的混合气体中所含的原子数目为0.1NA
- D、 含0.4molHCl的浓盐酸与足量MnO2反应,转移电子数目为0.2NA
试题详情  为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
- A、 0.1 mol/L
溶液中,含有
的数目为0.2
- B、 标准状况下,22.4 L
和22.4 L
在光照下充分反应后的分子数为2
- C、 1 mol
晶体和1 mol
晶体含有的离子数目均为2
- D、 一定条件下,5.6 g Fe与0.1 mol
充分反应,转移的电子数为0.3
试题详情
绿矾( )分解可制备铁红,同时产生
)分解可制备铁红,同时产生 、
、 和
和 。设NA为阿伏加德罗常数的值,下列说法错误的是
。设NA为阿伏加德罗常数的值,下列说法错误的是
- A、
溶液含有的阳离子数大于NA
- B、 0.5mol三聚
分子(
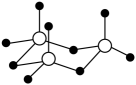 )中含有σ键数目为6 NA
)中含有σ键数目为6 NA - C、 绿矾分解生成16g
时,转移电子数为0.2 NA
- D、 22.4L
溶于水,溶液中
、
、
的数目总和为NA
试题详情
NA为阿伏加德罗常数的值。下列说法正确的是
- A、 22.4L 光气(COCl2) 所含分子数为NA
- B、 0.1 mol Cu(H2O)4SO4·H2O晶体中σ键数目为1.8 NA
- C、 电解1L饱和食盐水,pH=13时, 转移的电子数为0.05 NA
- D、 2mL5mol·L-1的硅酸钠溶液和盐酸反应后制得硅酸胶体,胶粒数为0.01NA
试题详情
设NA为阿伏加德常数的值,下列说法正确的是( )
- A、 1 mol Na2O2固体中含离子总数为4NA
- B、 标准状况下,22.4 L氨水含有NA个NH3分子
- C、 丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA
- D、 室温下,1 L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA
试题详情
NA表示阿伏加德罗常数,下列有关物质结构说法正确的是( )
- A、 NaH的电子式为:
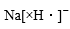
- B、 78克Na2O2晶体中所含阴阳离子总数为3NA
- C、 CCl4和PCl5分子中所有原子的最外层都达到了8电子稳定结构
- D、 浓硫酸溶于水电离出H+和SO
并放出大量的热,所以浓硫酸溶于水属于放热反应
试题详情
设NA表示阿伏加德罗常数的值,下列叙述中正确的是
- A、 含4.8g碳元素的石墨晶体中的共价键数是0.8NA
- B、 标准状况下,甲烷和氧气的混合气体共22.4L,完全燃烧后产物的分子总数可能为NA
- C、 10g的D2O中含有的质子数与中子数分别为5NA和4NA
- D、 常压、500℃、催化条件下,1molSO2和0.5molO2充入一密闭容器内,充分反应后的生成物分子数为NA
试题详情  为阿伏加德罗常数的值。下列叙述中正确的是
为阿伏加德罗常数的值。下列叙述中正确的是
- A、
中含有的
键的数目为
- B、 标准状况下,
和
在光照下充分反应后的分子数为
- C、
固体含有的离子数目为
- D、 一定条件下,5.6gFe与
充分反应,转移的电子数为
试题详情
设NA为阿伏加德罗常数的值,下列说法错误的是
- A、 标准状况下,2.24L丙烯中含有的σ键数目为0.8NA
- B、 6.0gSiO2与足量HF溶液充分反应,生成SiF4的数目为0.1NA
- C、 1.2gNaHSO4晶体中含有的
数目为0.01NA
- D、 5.6gFe与3.55g氯气充分反应后转移的电子数目为0.1NA
试题详情
设NA为阿伏加德罗常数的值,下列说法正确的是
- A、 1.0L1mol/LAlCl3溶液中,Al3+的数目为1.0NA
- B、 0.2mol苯含有双键的数目为0.6NA
- C、 电解熔融CuCl2 , 阴极增重3.2g,外电路中通过电子的数目为0.1NA
- D、 标准状况下22.4LSO3的质量为80g
试题详情  表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
- A、 一定条件下,5.6 g Fe与足量S反应,转移
个电子
- B、 常温下,
溶液中阴离子总数等于
- C、 电解精炼铜时每转移
个电子,阳极质量一定减少32 g
- D、 常温常压下,6 g
晶体中所含硅氧键数目为
试题详情
科学家发现某些生物酶能将海洋中的 转化为
转化为 , 该过程的总反应为
, 该过程的总反应为 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
- A、
溶液中含
离子的数目为
- B、 标准状况下,
中含
键的数目为
- C、 18克
中含电子对的数目为
- D、
完全反应失去电子的数目为
试题详情
甲酸甲酯常用作杀菌剂、熏蒸剂和烟草处理剂,可由甲酸和甲醇反应制得。NA为阿伏加德罗常数的值。下列有关说法正确的是
- A、 pH=3的甲酸溶液中氢离子数目为1×10-3NA
- B、 0.5 mol甲酸甲酯中含有sp3杂化的原子数目为NA
- C、 50g质量分数为64%的甲醇水溶液中含有σ键数目为5NA
- D、 甲醇燃料电池中,每消耗22.4L(标准状况)甲醇,转移电子数目为6NA
试题详情
设NA为阿伏加德罗常数的值,下列说法正确的是
- A、 标准状况下,生成2.24LO2转移的电子数为0.4NA
- B、 2L1mol·L-1的氯化铜溶液中H+数目为4NA
- C、 常温下,5.6g铁与足量稀硝酸反应转移的电子数为0.3NA
- D、 2LpH=5的0.05mol·L-1K2Cr2O7溶液中
数目为0.1NA
试题详情  为阿伏加德罗常数,下列叙述中正确的是( )
为阿伏加德罗常数,下列叙述中正确的是( )
- A、 常温常压下,
与
混合气体共含
个氧原子
- B、 标准状况下,22.4L乙烯中含有的
键数目为
- C、 密闭容器中,
与
充分反应生成HI(g),容器内分子数小于
- D、 常温下
与过量稀NaOH溶液反应,转移的电子总数为
试题详情
设 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
- A、
质量分数为46%的乙醇溶液中,含
键的数目为
- B、
晶体含有离子总数为
- C、 含
的浓硫酸与足量的镁反应,转移的电子数为
- D、 常温下,
的
溶液中,
的数目为
试题详情
设 是阿伏加德罗常数的值,催化氧化脱硫的工作原理:
是阿伏加德罗常数的值,催化氧化脱硫的工作原理: ,
,  时,
时, 。下列说法正确的是( )
。下列说法正确的是( )
- A、
水中含有的氢键数为2
- B、 每生成
,
失去的电子数为
- C、 氢氧化铁的悬浊液中,若
时,悬浊液中的
数目为
- D、 反应中每产生
, 消耗
数目
试题详情
利用电催化实现CO2到C2H5OH的转化,反应原理:6H2+2CO2 C2H5OH+3H2O。设NA为阿伏加德罗常数的值,下列有关说法正确的是( )
C2H5OH+3H2O。设NA为阿伏加德罗常数的值,下列有关说法正确的是( )
- A、 11.2L CO2中含分子的数目为0.5 NA
- B、 23gC2H5OH中含共价键的数目为4 NA
- C、 生成1 mol C2H5OH转移电子的数目为8 NA
- D、 4gH2与4gD2所含中子的数目相差NA

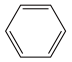 含有
含有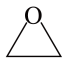 )中所含
)中所含
