选择题
试题详情
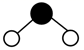
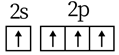
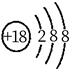
日光灯中用到的某种荧光粉的主要成分为3W3(ZX4)2·WY2。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
- A、 电负性:X>Y>Z>W
- B、 原子半径:X<Y<Z<W
- C、 Y和W的单质都能与水反应生成气体
- D、 Z元素最高价氧化物对应的水化物具有强氧化性
试题详情
W、X、Y、Z为原子序数依次增加的同一短周期元素,其中X、Y、Z相邻,W的核外电子数与X的价层电子数相等, 是氧化性最强的单质,4种元素可形成离子化合物
是氧化性最强的单质,4种元素可形成离子化合物 。下列说法正确的是
。下列说法正确的是
- A、 分子的极性:
- B、 第一电离能:X<Y<Z
- C、 氧化性:
- D、 键能:
试题详情
一种可吸附甲醇的材料,其化学式为 , 部分晶体结构如下图所示,其中
, 部分晶体结构如下图所示,其中 为平面结构。
为平面结构。
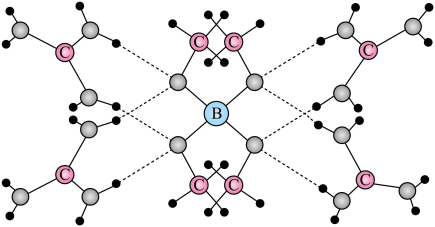
下列说法正确的是
- A、 该晶体中存在N-H…O氢键
- B、 基态原子的第一电离能:
- C、 基态原子未成对电子数:
- D、 晶体中B、N和O原子轨道的杂化类型相同
试题详情
X、Y、Z、M、Q五种短周期元素,原子序数依次增大。X的 轨道全充满,Y的s能级电子数量是p能级的两倍,M是地壳中含量最多的元素,Q是纯碱中的一种元素。下列说法错误的是
轨道全充满,Y的s能级电子数量是p能级的两倍,M是地壳中含量最多的元素,Q是纯碱中的一种元素。下列说法错误的是
- A、 电负性:
- B、 最高正价:
- C、 Q与M的化合物中可能含有非极性共价键
- D、 最高价氧化物对应水化物的酸性:
试题详情
阅读下列材料,完成5~7题:
周期表中IVA族元素及其化合物应用广泛。甲烷具有较大的燃烧热(890.3 kJ·mol-1),是常见燃料;Si、 Ge是重要的半导体材料,硅晶体表面SiO2能与氢氟酸(HF,弱酸)反应生成H2SiF6 (H2SiF6在水中完全电离为H+和SiF62- ); 1885年德国化学家将硫化锗(GeS2)与H2共热制得了门捷列夫预言的类硅-锗;我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜器;Pb、PbO2是铅蓄电池的电极材料,不同铅化合物一般具有不同颜色,历史上曾广泛用作颜料。
试题详情
利用反应 可制备N2H4。下列叙述正确的是( )
可制备N2H4。下列叙述正确的是( )
- A、 NH3分子有孤电子对,可做配体
- B、 NaCl晶体可以导电
- C、 一个N2H4分子中有4个σ键
- D、 NaClO和NaCl均为离子化合物,他们所含的化学键类型相同
试题详情  (锶)的
(锶)的 、
、 稳定同位素在同一地域土壤中
稳定同位素在同一地域土壤中 值不变。土壤生物中
值不变。土壤生物中 值与土壤中
值与土壤中 值有效相关。测定土壤生物中
值有效相关。测定土壤生物中 值可进行产地溯源。下列说法错误的是( )
值可进行产地溯源。下列说法错误的是( )
- A、
位于元素周期表中第六周期、第ⅡA族
- B、 可用质谱法区分
和
- C、
和
含有的中子数分别为49和48
- D、 同一地域产出的同种土壤生物中
值相同
试题详情  、
、 的半衰期很短,自然界中不能稳定存在。人工合成反应如下:
的半衰期很短,自然界中不能稳定存在。人工合成反应如下: ;
; 。下列说法正确的是( )
。下列说法正确的是( )
- A、 X的中子数为2
- B、 X、Y互为同位素
- C、
、
可用作示踪原子研究化学反应历程
- D、 自然界不存在
、
分子是因其化学键不稳定
试题详情
化合物 可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子序数依次增加,且加和为21。
可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子序数依次增加,且加和为21。 分子的总电子数为奇数,常温下为气体。该化合物的热重曲线如图所示,在
分子的总电子数为奇数,常温下为气体。该化合物的热重曲线如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是( )
以下热分解时无刺激性气体逸出。下列叙述正确的是( )
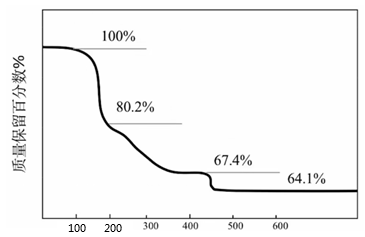
- A、 W、X、Y、Z的单质常温下均为气体
- B、 最高价氧化物的水化物的酸性:
- C、
阶段热分解失去4个
- D、
热分解后生成固体化合物
试题详情
甲烷单加氧酶(s—mmo)含有双核铁活性中心,是O2氧化CH4生成CH3OH的催化剂,反应过程如图所示。下列叙述错误的是( )

- A、 基态Fe原子的核外电子排布式为[Ar]3d64s2
- B、 步骤③有非极性键的断裂和极性键的形成
- C、 每一步骤都存在铁和氧元素之间的电子转移
- D、 图中的总过程可表示为:CH4+O2+2H++2e-
CH3OH+H2O
试题详情
某多孔储氢材料前驱体结构如图,M、W、X、Y、Z五种元素原子序数依次增大,基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法正确的是( )

- A、 氢化物沸点:
- B、 原子半径:
- C、 第一电离能:
- D、 阴、阳离子中均有配位键
试题详情
单质硫和氢气在低温高压下可形成一种新型超导材料,其晶胞如图。下列说法错误的是( )

- A、 S位于元素周期表p区
- B、 该物质的化学式为
- C、 S位于H构成的八面体空隙中
- D、 该晶体属于分子晶体
试题详情
SF6可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关SF6的说法正确的是( )
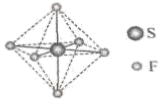
- A、 是非极性分子
- B、 键角
都等于90°
- C、
与
之间共用电子对偏向S
- D、
原子满足8电子稳定结构
试题详情
“天问一号”着陆火星,“嫦娥五号”采回月壤。腾飞中国离不开化学,长征系列运载火箭使用的燃料有液氢和煤油等化学品。下列有关说法正确的是( )
- A、 煤油是可再生能源
- B、
燃烧过程中热能转化为化学能
- C、 火星陨石中的
质量数为20
- D、 月壤中的
与地球上的
互为同位素
非选择题
试题详情
中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物( )。回答下列问题:
)。回答下列问题:
试题详情
硅材料在生活中占有重要地位。请回答:
试题详情
工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为: 。回答下列问题:
。回答下列问题:
试题详情
1962年首个稀有气体化合物 问世,目前已知的稀有气体化合物中,含氙(54Xe)的最多,氪 (36Kr)次之,氩(18Ar)化合物极少。
问世,目前已知的稀有气体化合物中,含氙(54Xe)的最多,氪 (36Kr)次之,氩(18Ar)化合物极少。 是
是 与
与 分子形成的加合物,其晶胞如下图所示。
分子形成的加合物,其晶胞如下图所示。

回答下列问题:
试题详情
【选考题】配位化合物X由配体L2-(如图)和具有正四面体结构的[Zn4O]6+构成。

试题详情
【选修3:物质结构与性质】
含Cu、Zn、Sn及S的四元半导体化合物(简写为CZTS),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
试题详情
金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
试题详情
工业中可利用生产钛白的副产物 和硫铁矿
和硫铁矿 联合制备铁精粉
联合制备铁精粉 和硫酸,实现能源及资源的有效利用。
和硫酸,实现能源及资源的有效利用。
试题详情
以 、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
试题详情
研究笼形包合物结构和性质具有重要意义。化学式为 的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数为
的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数为 。回答下列问题:
。回答下列问题:
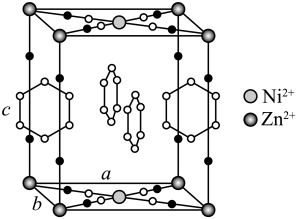
试题详情
[选修3:物质结构与性质]
铁和硒( )都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用。回答下列问题:
试题详情
硒(  )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(  )效应以来,
)效应以来,  在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含  的新型
的新型  分子
分子  的合成路线如下:
的合成路线如下:

试题详情
[化学——选修3:物质结构与性质]
卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
试题详情
铁单质及其化合物的应用非常广泛。
试题详情
金属羰基配位化合物在催化反应中有着重要应用。HMn(CO)5是锰的一种简单羰基配位化合物,其结构示意图如下。
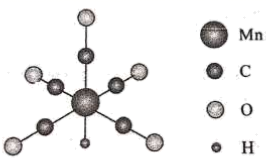
回答问题:
试题详情
非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
试题详情
[选修3:物质结构与性质]
很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物I可与氧化汞生成化合物Ⅱ。
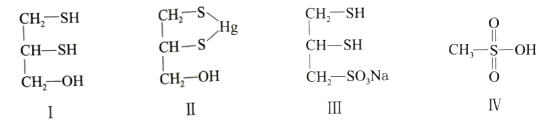
试题详情
[化学-选修3:物质结构与性质]
我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
试题详情
[选修3:物质结构与性质]
硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
试题详情
[选修3:物质结构与性质]
KH2PO4晶体具有优异的非线性光学性能。我国科学工作者制备的超大KH2PO4晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
试题详情
[化学——选修3:物质结构与性质]
过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用,回答下列问题:

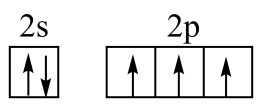

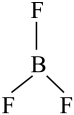 (平面三角形)
(平面三角形)