选择题
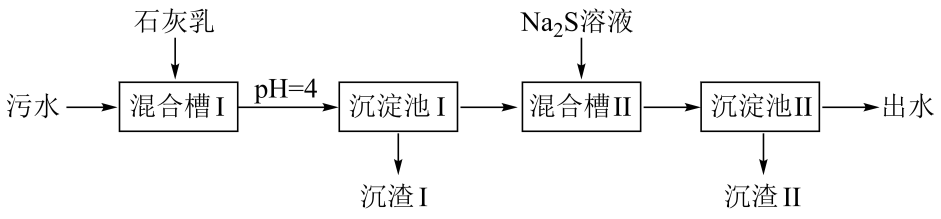
已知:①溶液中金属离子开始沉淀和完全沉淀的如下表所示:
| 物质 | | | | |
| 开始沉淀 | 1.9 | 4.2 | 6.2 | 3.5 |
| 完全沉淀 | 3.2 | 6.7 | 8.2 | 4.6 |
②。
下列说法错误的是
- A、 “沉渣Ⅰ”中含有
和
- B、
溶液呈碱性,其主要原因是
- C、 “沉淀池Ⅱ”中,当
和
完全沉淀时,溶液中
- D、 “出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水
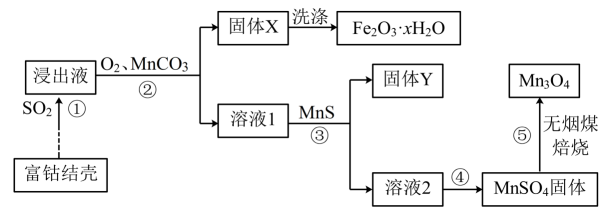
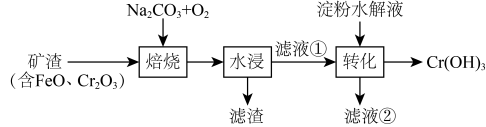
已知:①“浸出液”中主要含有的金属离子为:;
②温度高于时,
在水中的溶解度随温度升高迅速降低;
③“焙烧”的过程发生的部分反应有 ,
下列有关说法错误的是( )
- A、 过程②中,
和
的作用分别是氧化剂和沉淀剂
- B、 固体Y中主要物质的化学式为
- C、 过程④中的操作是蒸发浓缩、冷却结晶、过滤、洗涤、干燥
- D、 流程中可循环使用的物质有
- A、 逐滴滴入
的目的是提高双氧水的利用率
- B、 温度维持在
的理由之一是防止
分解
- C、 使用磁力搅拌器的目的是为了提高
平衡产率
- D、 常压蒸馏可以分离提纯
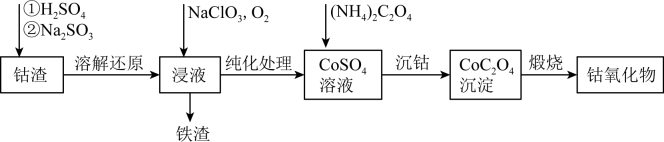
已知:
下列说法正确的是( )
- A、 “溶解还原”过程中得到的
与消耗的
物质的量之比为
- B、 “沉钴”时,不用
溶液是为了防止溶液碱性太强而生成
沉淀
- C、 可以用氢氧化钠溶液检验
固体是否洗涤干净
- D、 “焙烧”的方程式为
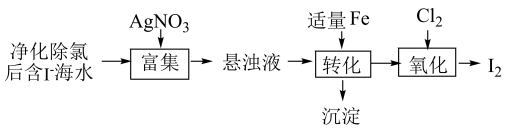
下列说法错误的是
- A、 “富集”中所发生的离子反应为:
- B、 “转化”中为了使悬浊液充分反应,使用铁粉并搅拌
- C、 “转化”中生成的沉淀与硝酸反应所得产物可循环使用
- D、 “氧化”中通入足量氯气时只得到氧化产物
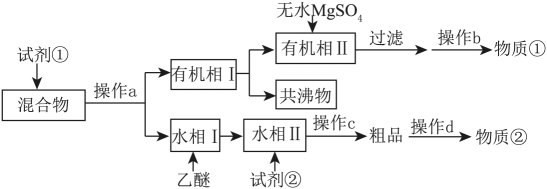
已知:苯甲酸乙酯的沸点为212.6℃,乙醚-环己烷-水共沸物的沸点为62.1℃,苯甲酸100℃会迅速升华
- A、 试剂①为饱和Na2CO3溶液,试剂②为稀硫酸
- B、 操作a、c均为分液,操作b为蒸馏,操作d为重结晶
- C、 苯甲酸乙酯、苯甲酸分别由①②获得
- D、 粗品精制还可以用升华法

已知:苯甲酸乙酯的沸点为212.6℃,“乙醚-环己烷-水共沸物”的沸点为62.1℃。下列说法错误的是
- A、 操作a和操作b不同
- B、 操作c为重结晶
- C、 无水
和饱和碳酸钠溶液的作用相同
- D、 由该流程可以说明苯甲酸和苯甲酸钠在水中的溶解度差别很大
- A、 “凡酸坏之酒,皆可蒸烧”,该过程利用了物质的溶解性不同
- B、 “青蒿一握,以水二升渍,绞取汁”,青蒿素的提取过程涉及化学变化
- C、 “风干日曝咸味加,始灌潮波塯成卤”,该过程涉及的操作方法是蒸发结晶
- D、 “凡石灰,经火焚炼为用 ……火力用后,烧酥石性,置于风中,久自吹成粉”中的“粉”为CaO

- A、 “过滤”可除去未反应的铁粉
- B、 “除杂”使用饱和NaHSO3溶液可除去剩余的溴单质
- C、 “干燥”时可使用浓硫酸作为干燥剂
- D、 “蒸馏”的目的是分离苯和溴苯
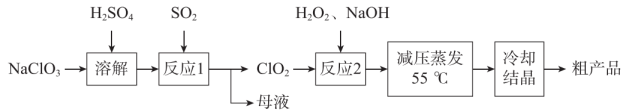
下列说法错误的是
- A、 “母液”中主要成分是
- B、 “反应2”中氧化剂与还原剂的物质的量之比为
- C、 “减压蒸发”可以降低蒸发时的温度,提高产品产率
- D、 以生成
时转移电子数目来衡量,相同质量
的消毒能力是
的2.5倍

已知:溶液在加热时易分解产生
和
;“溶解”工序发生的反应为可逆反应。下列说法错误的是
- A、 “氧化”时,适宜选择水浴加热方式
- B、 若省略第一次过滤,会使氨水的用量增加
- C、 滤渣Ⅱ洗涤后的滤液可送入“还原”工序利用
- D、 “还原”时,每生成
, 理论上消耗
- A、 ①中消耗
转移
- B、 ②中溶液先变浑浊的原因:2Na2S+3SO2= 2Na2SO3+3S↓
- C、 为提高产品的纯度,混合液中
的最佳比例为1∶2
- D、 用适量
溶液吸收②中选出的
、
气体,吸收液可直接返回到步骤②
多选题

流程中几种物质的沸点如表
物质 | ||||
沸点 | 136 | 127 | 57 | 180 |
非选择题
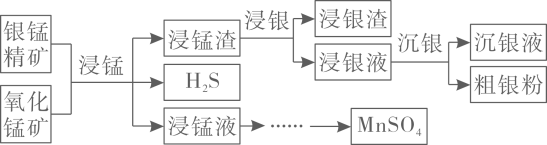
已知:酸性条件下,的氧化性强于
。
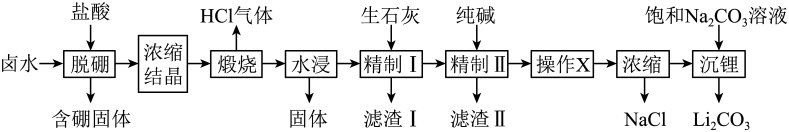
已知:常温下,。相关化合物的溶解度与温度的关系如图所示。

回答下列问题:

已知:①金属的化学性质和
相似,
的熔点为
;
②(乙醚)和
(三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:
| 物质 | | | | |
| 沸点/ | 55.7 | 34.6 | 42.4 | 365.8 |
回答下列问题:
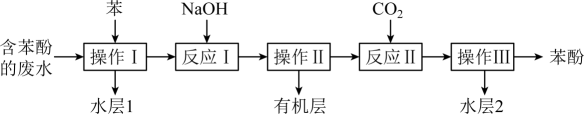
回答下列问题:

已知:①辉铜矿主要含有Cu2S及少量SiO2、 Fe2O3等杂质,软锰矿主要含有MnO2及少量SiO2、Fe2O3等杂质。
②S在CS2中的溶解度随温度升高而增大;CS2的沸点为46.2 ℃。
③[ Cu(NH3)4]2+(aq)Cu2+ (aq) + 4NH3(aq)
请回答下列问题:

已知:①单宁酸是一种只含C、H、O元素的有机化合物
② , 常温下
,
,
,
③当溶液中某离子的物质的量浓度不大于时,该离子沉淀完全
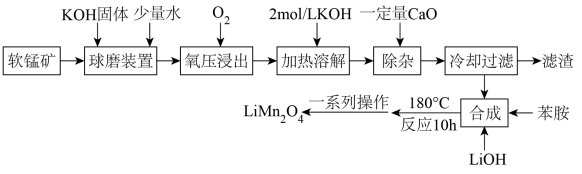
已知:
①软锰矿的成分如下:
| 成分 | MnO2 | Fe2O3 | CaO | SiO2 | 其他不反应杂质 |
| 质量分数 | 69.6% | 7.6% | 5.6% | 9.0% | 8.2% |
②K2MnO4在强碱性溶液(pH大于13.5)中稳定,在酸性、中性和弱碱性环境中会发生歧化反应生成和MnO2。
③苯胺(C6H5NH2)还原性较强,在该条件下可被氧化为硝基苯(C6H5NO2)。
④锰酸锂为灰黑色粉末,离子化合物,易溶于水,难溶于无水乙醇。

回答下列问题

已知:
①酸浸后As元素以H3AsO4形式存在;
②常温下,Ksp[Cu(OH)2]≈1.0×10-20;
③聚合硫酸铁盐基度[聚合硫酸铁中×100%]越大,絮凝效果越好。
回答下列问题:

资料:一些物质的(25℃)如下。
物质 | ||||

已知:萃取时发生的反应为。


已知:① ,
;②溶液中某离子浓度
时,认为该离子沉淀完全;③室温时生成氢氧化物的pH见下表
离子 | |||||
开始沉淀的pH | 7.5 | 2.7 | 8.1 | 7.7 | 8.3 |
完全沉淀的pH | 9.7 | 3.7 | 9.4 | 8.4 | 9.8 |
回答下列问题:

回答下列问题:

已知:25℃。 ,
。
请回答下列问题:

室温下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
开始沉淀时(c=0.01mol·L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时(c=1.0×10-5mol·L-1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
回答下列问题:

已知:①NH4VO3难溶于水,(VO2)2SO4易溶于水;
② +2H+
+ H2O;
③几种金属离子以氢氧化物沉淀时的pH如下表。
金属氢氧化物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
开始沉淀的pH | 2.7 | 4.0 | 4.6 |
完全沉淀的pH | 3.7 | 5.2 | 6.0 |
请回答下列问题: