选择题
选项 | 实验操作和和现象 | 结论 |
A | 取足量 | 则说明盐酸有剩余 |
B | 某溶液中滴加过量的氨水产生白色沉淀 | 则说明溶液中含 |
C | 向某溶液中加入少量 | 则说明溶液中不含 |
D | 将两支盛有等体积、等浓度的 | 则说明其他条件相同时,升高温度能加快反应速率 |
- A、 A
- B、 B
- C、 C
- D、 D
选项 | 探究方案 | 探究目的 |
A | 向试管中滴入几滴1-溴丁烷,再加入 | 检验1-溴丁烷中的溴元素 |
B |
| 乙醇发生了消去反应 |
C | 取2%硫酸铜溶液2mL再加入2%NaOH溶液1mL,再加入少量乙醛加热至沸腾,产生砖红色沉淀 | 醛基能被新制的 |
D | 向苯和少量苯酚的混合溶液中加入足量的浓溴水,充分反应后,过滤 | 除去苯中少量的苯酚杂质 |
- A、 A
- B、 B
- C、 C
- D、 D
选项 | 实验及现象 | 结论 |
A | 将2-溴丙烷与NaOH的乙醇溶液共热,产生的气体通入酸性高锰酸钾溶液,溶液褪色 | 2-溴丙烷发生了消去反应 |
B | 向电石中逐滴加入饱和食盐水,将产生的气体通入溴水中,溴水褪色 | 乙炔与Br2发生了加成反应 |
C | 将铜丝烧至表面变黑,伸入盛有某有机物的试管中,铜丝恢复亮红色 | 该有机物中一定含有醇羟基 |
D | 将石蜡油加强热,产生的气体通入Br2的四氯化碳溶液,溶液褪色 | 产生的气体中含有不饱和烃 |
- A、 A
- B、 B
- C、 C
- D、 D
选项 | 实验操作和实验现象 | 结论 |
A | 在一块除去铁锈的铁片上滴1滴含有酚酞的食盐水静置2~3min,溶液边缘出现红色 | 铁片上发生了吸氧腐蚀 |
B | 将足量H2O2溶液滴入少量的酸性高锰酸钾溶液溶液紫色褪去 | H2O2具有漂白性 |
C | 向某溶液中滴加NaOH溶液并将湿润的红色石蕊试纸置于试管口,试纸颜色无明显变化 | 原溶液中无 |
D | 向Na2CO3、Na2S的混合溶液中滴入少量AgNO3溶液,有黑色沉淀生成 | Ksp(Ag2S)<Ksp(Ag2CO3) |
- A、 A
- B、 B
- C、 C
- D、 D

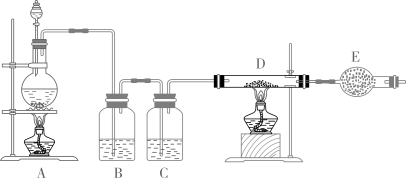
- A、 A装置中的药品可替换成铜片和浓硫酸
- B、 B装置可作储气瓶和安全瓶
- C、 C装置中溶液变浑浊,说明SO2具有氧化性
- D、 E中可选用NaOH溶液除去尾气
选项 | 实验操作 | 实验现象 | 实验结论 |
A | 向淀粉KI溶液中滴入适量稀硫酸 | 溶液变蓝 | 稀硫酸将I-氧化为I2 |
B | 向AgCl悬浊液中滴入适量氨水 | 悬浊液变澄清 | AgCl(s) |
C | 加热NH4Cl固体 | 产生刺激性气味的气体 | 加热NH4Cl可制备NH3 |
D | 向酸性KMnO4溶液中滴入H2C2O4溶液 | 酸性KMnO4溶液褪色 | H2C2O4具有漂白性 |
- A、 A
- B、 B
- C、 C
- D、 D
选项 | 实验操作和现象 | 实验结论 |
A | 卤代烃Y与NaOH水溶液共热后,再滴入 | 说明卤代烃未水解 |
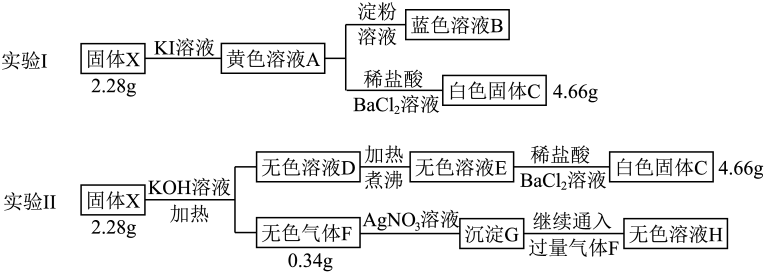
B | 取 | 则KI与 |
C | 向溶有 | X可能是 |
D | 测得 | |
- A、 A
- B、 B
- C、 C
- D、 D
多选题

已知:①“焙烧”后,碲主要以形式存在;“氧化”过程,Te被氧化为+6价
②微溶于水,易溶于强酸和强碱,与强碱生成
选项 | 实验操作 | 实验现象 | 结论 |
A | 将NaOH溶液逐滴滴加到 | 先产生白色胶状沉淀,后沉淀溶解 |
|
B | 测定等浓度的 | 前者pH比后者大 | 非金属性:S>C |
C | 向2.0mL浓度均为 | 沉淀呈黄色 | |
D | 分别向两支盛有 | 前者产生无色气泡,后者无明显现象 | 酸性:醋酸>碳酸>硼酸 |
非选择题
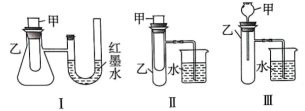
实验装置及操作 |
|
|
|
实验现象 | 盛有 (填化学式)试管中温度计示数升高 | 盛有 | |
实验结论或解释 | 相同温度下,溶解度: |
|

已知:常温下, ,
。回答下列问题:

回答下列问题:

猜测1:发生复分解反应。
猜测2:与
发生氧化还原反应。
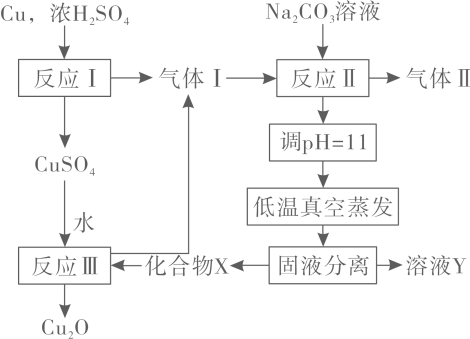
请回答:
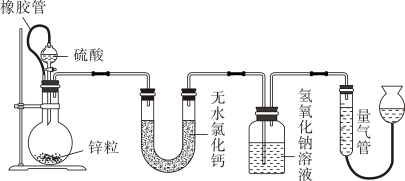
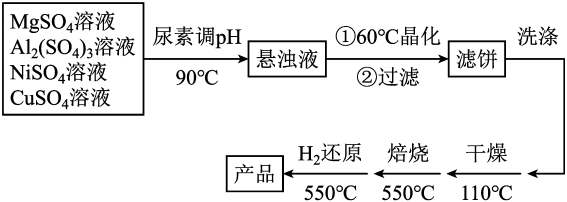
请回答:

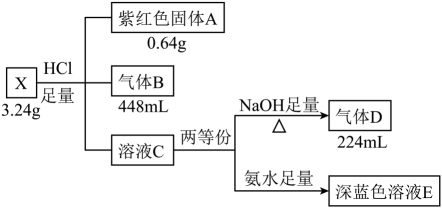
已知:上述气体体积均在标准状况下测得。气体B为纯净物,有刺激性气味,标准状况下密度为2.86 g/L。请回答:

 制SO2
制SO2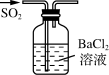 制BaSO3沉淀
制BaSO3沉淀 验证SO2的还原性
验证SO2的还原性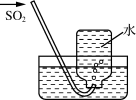 收集SO2
收集SO2



