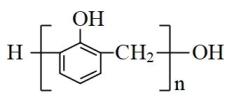
选择题
- A、 灼烧法做“海带中碘元素的分离及检验”实验时,须将海带进行灰化
- B、 用纸层析法分离铁离子和铜离子时,不能将滤纸条上的试样点浸入展开剂中
- C、 将盛有苯酚与水形成的浊液的试管浸泡在80℃热水中一段时间,浊液变澄清
- D、 不能将实验室用剩的金属钠块放回原试剂瓶
- A、 酚酞滴入醋酸钠溶液中变为浅红色:CH3COO-+H2O⇌CH3COOH+OH-
- B、 金属钠在空气中加热生成淡黄色固体:4Na+O2=2Na2O
- C、 铝溶于氢氧化钠溶液,有无色气体产生:2Al+2OH-+2H2O=2
+3H2↑
- D、 将二氧化硫通入氢硫酸中产生黄色沉淀:SO2+2H2S=3S↓+2H2O
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究乙醇消去反应的产物 | 取 | 若溴水褪色,则乙醇消去反应的产物为乙烯 |
| B | 探究乙酰水杨酸样品中是否含有水杨酸 | 取少量样品,加入 | 若有紫色沉淀生成,则该产品中含有水杨酸 |
| C | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入 | 若无气体生成,则固体粉末为 |
| D | 探究 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量 | 若有白色沉淀产生,则样品已经变质 |
- A、 A
- B、 B
- C、 C
- D、 D
- A、 室温下,Na在空气中反应生成Na2O2
- B、 室温下,Al与4.0 mol﹒L-1NaOH溶液反应生成NaAlO2
- C、 室温下,Cu与浓HNO3反应放出NO气体
- D、 室温下,Fe与浓H2SO4反应生成FeSO4
- A、 Fe在稀硝酸中发生钝化
- B、 MnO2和稀盐酸反应制取Cl2
- C、 SO2与过量氨水反应生成(NH4)2SO3
- D、 室温下Na与空气中O2反应制取Na2O2
- A、 元素的非金属性越强,简单氢化物的酸性越弱
- B、 由金属活动性顺序可知,钙比钠与水反应更剧烈
- C、 碳酸氢钠和碳酸钠均可用作食品膨松剂
- D、
与浓硫酸和稀硫酸反应时,硫酸同时体现酸性和氧化性
- A、 利用合适的催化剂可减少汽车尾气中有害气体的排放
- B、 钠着火可用泡沫灭火器灭火
- C、 高纯硅可用于制作光感电池
- D、 疫苗一般冷藏存放,以避免蛋白质变性
- A、 中华酒文化源远流长,酿酒过程中涉及水解反应、氧化反应等多种反应类型
- B、 我国已能利用3D打印技术,以钛合金粉末为原料,通过激光熔化逐层堆积,来制造机钛合金结构件;高温时可用金属钠还原相应的氯化物来制取金属钛
- C、 新冠疫情席卷全球,目前使用的一次性医用口罩(SMS),其原料是聚丙烯,能使溴水或酸性高锰酸钾溶液褪色
- D、 垃圾分类很重要,充电电池和硒鼓墨盒都属于有害垃圾
- A、 滴有酚酞的碳酸钠溶液呈红色:CO
+2H2O
H2CO3+2OH-
- B、 在空气中加热金属钠生成淡黄色固体:2Na+O2
Na2O2
- C、 氢氧化铝溶于氢氧化钠溶液:Al(OH)3+OH-=AlO
+2H2O
- D、 将氯气通入氢硫酸中产生黄色沉淀:H2S+Cl2=S↓+2HCl
选项 | 实验操作 | 现象 |
A | 向溴的氯仿溶液中通入足量乙烯 | 溴的氯仿溶液颜色逐渐变浅,最终变为无色 |
B | 向淀粉溶液中先加入足量稀硫酸,再加入少量新制氢氧化铜悬浊液,加热 | 产生砖红色沉淀 |
C | 向盛有大量水的烧杯中加入少量钠块 | 钠块熔化成银白色小球 |
D | 常温下,向AgCl浊液中加入KI浓溶液,振荡已知:[Ksp(AgCl)>Ksp(AgI)] | 白色浊液变成淡黄色浊液(或沉淀) |
- A、 A
- B、 B
- C、 C
- D、 D
- A、 纸层析法分离Fe3+和Cu2+ , 氨熏后纸条上端为棕红色,下端为深蓝色
- B、 从海带中提取碘的工业生产过程步骤:灼烧、浸泡、过滤、氧化、结晶、提纯
- C、 培养明矾晶体时,将小晶体悬挂在90℃热饱和溶液的烧杯中央,自然冷却至室温
- D、 金属钾、钠和白磷暴露空气中易燃烧,均应保存在煤油中
- A、 Na与H2O反应生成NaOH和H2 , 则Fe与H2O反应生成Fe(OH)3和H2
- B、 CO2可与水反应生成H2CO3 , 则SiO2可与水反应生成H2SiO3
- C、 铁与硫加热反应生成FeS,则铜与硫加热反应生成Cu2S
- D、 Cl2与H2O反应生成HCl和HClO,则F2与H2O反应生成HF和HFO
- A、 钠单质熔点较低,可用于冶炼金属钛
- B、 次氯酸钠具有强氧化性,可用作环境消毒剂
- C、 氢氧化钠具有强碱性,可用作干燥剂
- D、 碳酸氢钠受热易分解,可用于泡沫灭火器
| 实验 | 现象 | 结论 | |
| A | 将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶 | 集气瓶中产生大量白烟,瓶内有黑色颗粒产生 | CO2具有氧化性 |
| B | 缓缓加热0.5mol·L-1CH3COONa溶液到60℃,并用pH传感器测定溶液的pH | 溶液的pH逐渐减小 | 溶液中c(H+)逐渐增大,c(OH-)逐渐减小 |
| C | 温下,将50mL苯与50mLCH3COOH混合 | 所得混合溶液的体积为101mL | 混合过程中削弱了CH3COOH分子间的氢键,且苯与CH3COOH分子间的作用弱于氢键 |
| D | 利用电导仪测定碱性条件下乙酸乙酯水解反应中电导率的变化(溶液温度不变) | 随着反应进行,电导率逐渐减小 | OH-的电导大于CH3COO-的电导 |
- A、 A
- B、 B
- C、 C
- D、 D
| 选项 | 实验操作和现象 | 结论 |
| A | 某SO2气体中可能存在CO2 , 将气体依次通过NaHCO3溶液、品红溶液、澄清石灰水,品红溶液不褪色,澄清石灰水变浑浊 | 该气体中存在CO2 |
| B | 去家用食盐少量,溶于水,加少量淀粉固体,充分搅拌,无明显变化 | 这是一种没有添加碘的食盐 |
| C | 取细铁丝在酒精灯上灼烧至红热,再伸入充满氯气的瓶中,剧烈反应,产生大量红褐色的烟,结束后,加水振荡,使固体充分溶解,再滴加2滴KSCN溶液,溶液未变色 | Fe再Cl2中燃烧生成FeCl2 |
| D | 将钠块融化后,上面倒扣一个充满CO2的集气瓶,剧烈燃烧,产生大量白烟,瓶壁有黑色固体 | 钠置换产生了碳单质 |
- A、 A
- B、 B
- C、 C
- D、 D
| 选项 | 操作 | 现象 | 结论 |
| A | 向某溶液中依次摘入几滴KSCN溶液和新制氯水 | 溶液先无明显现象,后变红 | 该溶液中含Fe2+ |
| B | 将一小块金属钠放在蒸发皿里,加热 | 发出黄色火焰,生成淡黄色固体 | 金属钠在空气中加热生成过氧化钠 |
| C | 用排水法收集铜和稀硝酸加热产生的气体 | 集气瓶中充满红棕色气体 | 反应生成红棕色气体且不溶于水 |
| D | 向1mL0.1mol•L-1NaOH溶液中依次滴入2滴浓度均为0.1mol•L-1的MgCl2溶液和FeCl3溶液 | 先产生白色沉淀,后生成红褐色沉淀 | 相同温度下:Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
- A、 A
- B、 B
- C、 C
- D、 D
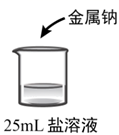
查阅资料:溶液中离子的浓度越大,离子所带的电荷数目越多,溶液的离子强度越大。
| 实验 | 序号 | 盐溶液 | 现象 |
| | ① | | 与钠与水的反应类似,钠熔化成一个闪亮的小球,四处游动,速度较快,没有火花出现 |
| ② | 2.0mol/LKCl溶液 | 反应比①剧烈,没有火花出现 | |
| ③ | | 反应比②剧烈,没有火花出现 | |
| ④ | | 反应瞬间即有黄色火花出现,并立即发生剧烈燃烧 |
- A、 由①②可知,随着KCl溶液浓度的增加,钠与KCl溶液的反应速率明显加快
- B、 实验③比②反应更加剧烈,一定是因为钠与碳酸根离子发生氧化还原反应
- C、 实验④中出现燃烧现象,是因为钠与水、与硝酸根离子发生了氧化还原反应,导致反应放出大量的热,达到了钠的着火点
- D、 推测若采用
溶液进行上述实验,也会出现钠的燃烧现象
- A、 CuSO4稀溶液与Na反应析出Cu
- B、 Fe与水蒸气在高温下反应生成Fe2O3
- C、 SO2的水溶液与溴蒸气反应富集溴
- D、 饱和食盐水与通入的NH3、CO2反应析出Na2CO3固体
- A、 工业上,在高温熔融、隔绝空气的条件下,利用钠单质和钛、钽等金属的氧化物发生置换反应,来制备钛、钽等稀有金属材料
- B、 铁的化合物应用十分广泛,氯化铁、硫酸亚铁是优良的净水剂
- C、 铜丝在氯气中燃烧,产生大量棕色的烟,实验结束后在集气瓶中加入少量水,盖上玻片后充分振荡,棕色消失,得到绿色溶液,再加水稀释,最终得到蓝色溶液
- D、 工业上锌可用湿法冶炼——电解 ZnSO4 溶液制备 Zn
| 实验 | 现象 | 结论 | |
| A. | 向2mL0.1mol/LFeCl3的溶液中加足量铁粉,振荡,加1滴KSCN溶液 | 黄色逐渐消失,加KSCN溶液颜色不变 | 还原性:Fe>Fe2+ |
| B. | 将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶 | 集气瓶中产生大量白烟,瓶内有黑色颗粒产生 | CO2具有氧化性 |
| C. | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3显碱性 |
| D. | 将SO2通入酸性KMnO4溶液 | 紫色溶液褪色 | SO2具有还原性 |
- A、 A
- B、 B
- C、 C
- D、 D
①金属钠投入到FeCl2溶液中 ②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④向饱和Na2CO3溶液中通入过量CO2 .
- A、 ①②③④
- B、 ①④
- C、 ③④
- D、 ②③
- A、 铁、锰、铬以及它们的合金称为黑色金属材料
- B、 用铬酸作氧化剂可以使铝表面的氧化膜产生美丽的颜色
- C、 可溶性铜盐有毒,但在生命体中,铜是一种不可缺少的微量元素
- D、 钠与水反应、镁与沸水反应、红热的铁与高温水蒸气反应均生成碱和氢气