选择题

- A、 H2O2的电子式为
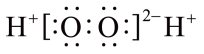
- B、 反应①②③均为氧化还原反应
- C、 反应②中有1molO2参与反应时转移电子的物质的量为2mol
- D、 反应过程中[PbCl2O2]2−、HCl均为该反应的催化剂

- A、 H2O2是一种绿色消毒剂,在消毒过程中消耗34gH2O2时反应转移1mol电子
- B、 该制备反应的总反应方程
- C、 该过程中1mol微粒含电子数为18NA的粒子有3种
- D、 反应过程中每一步反应Pd元素的化合价均发生了变化
- A、 Na2S2与盐酸反应生成NaCl、S和H2S,则S2Cl2在盐酸中转化为HCl、S和H2S
- B、 Na2O2具有较强的氧化性,则Na2S2也具有氧化性,但比Na2O2弱
- C、 H2O2易分解为H2O和O2 , 则H2S2也易分解为H2S和S
- D、 H2O2的分子构型不是直线形,则S2Cl2也不是直线形
- A、 硅酸钠溶液和盐酸反应:
- B、 硫酸铜溶液中加少量的铁粉:
- C、 酸性碘化钾溶液中滴加适量双氧水:
- D、 二氧化硫与酸性高锰酸钾溶液反应:
- A、 过碳酸钠具有强氧化性
- B、 1mol过碳酸钠发生热分解,转移的电子数为3NA
- C、 生产过种中若遇到酸、铁盐等都可能导致产率下降
- D、 将过碳酸钠溶液与亚硫酸氢钠溶液混合,发生的反应为2Na2CO3·3H2O2+3NaHSO3=2Na2CO3+3NaHSO4+3H2O
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究Fe2+、Cu2+对H2O2溶液分解的催化效果强弱 | 在两支试管a、b中各加2 mL5%H2O2溶液,分别滴入0.1 mol•L-1FeCl3溶液和0.1 mol•L-1CuSO4溶液各0.5 mL | 若a中产生气泡快于b中,则说明Fe3+的催化效果强于Cu2+ |
| B | 探究Fe与水蒸气高温反应后固体产物中铁元素的化合价 | 取少量固体产物于试管中,加足量的稀硫酸溶解,分成两份:一份滴加几滴KSCN溶液,另一份少量滴加KMnO4溶液 | 若前者溶液变血红色,后者溶液紫色褪去,则固体产物中铁元素有+2、+3两种价态 |
| C | 探究油脂在碱性条件下的水解 | 在小烧杯中加入约5 g动物脂肪、6 mL95%的乙醇,再加入6 mL 40%的氢氧化钠溶液,微热一段时间后取少量清液,加入新制氢氧化铜 | 若出现绛蓝色,则油脂已发生水解 |
| D | 探究Cu与硫酸的 反应 | 铜粉加入稀硫酸中,加热,再加入少量KNO3固体 | 未加KNO3固体前,无明显现象;加入KNO3固体后,产生大量气泡,则说明KNO3起催化作用 |
- A、 A
- B、 B
- C、 C
- D、 D
| 选项 | 实验操作和现象 | 结论 |
| A | 向H2O2溶液中滴加少量KMnO4溶液,紫红色褪去 | H2O2具有氧化性 |
| B | 将二氧化硫气体通入品红溶液,品红溶液褪色 | 二氧化硫具有漂白性 |
| C | 向蔗糖中滴入浓硫酸,固体变黑膨胀 | 浓硫酸具有吸水性 |
| D | AgCl悬浊液中滴入稀KI溶液,有黄色沉淀出现 | KSPAgI > KSPAgCl |
- A、 A
- B、 B
- C、 C
- D、 D
- A、 石灰石可用作燃煤的脱硫剂
- B、 过氧化氢溶液可用作医用消毒剂
- C、 碳酸钡可用作胃肠X射线透视的造影剂
- D、 硫化钠可用作去除废水中Pb2+的沉淀剂

- A、 H2O参与了该催化反应
- B、 过程①中反应的原子利用率为100%
- C、 该催化循环过程中有氢氧键的断裂和形成
- D、 每次循环的净反应为H2O2+2Cl-=2HOCl+2e-
| 选项 | 操作 | 现象 | 结论 |
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状炭,并放出有刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
| B | 向 KCl、KI 的混合液中逐滴滴加稀 AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 铝片先用砂纸打磨,再加入到浓硝酸中 | 无明显现象 | 浓硝酸具有强氧化性,常温下,铝表面被浓硝酸氧化为致密的氧化铝薄膜 |
| D | 向盛有 H2O2 溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后溶液中出现气泡,随后有红褐色沉淀生成 | Fe3+催化 H2O2 分解产生 O2 |
- A、 A
- B、 B
- C、 C
- D、 D
| 实验操作 | 实验现象 | 结论 | |
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状炭,并放出有刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
| B | 向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后溶液中出现气泡,随后有红褐色沉淀生成 | Fe3+催化H2O2分解产生O2 |
| C | 铝片先用砂纸打磨,常温下再加入到浓硝酸中 | 无明显现象 | 常温下,铝不跟浓硝酸反应 |
| D | 向浓度均为0.01mol·L-1的KCl、KI的混合液中逐滴滴加稀AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
- A、 A
- B、 B
- C、 C
- D、 D
①用于消毒的酒精、“84”消毒液、双氧水、过氧乙酸(CH3COOOH)等均属于有机物
②95%的酒精比75%的酒精杀菌效果好
③“84”消毒液露置在空气中不会变质
④双氧水能使酸性高锰酸钾溶液和溴水褪色,其褪色原理均为氧化还原反应
⑤修建“火神山”医院所用的HDPE(高密度聚乙烯)膜是一种无毒、无味的高分子材料
⑥医用外科口罩和防护服所用的熔喷布是一种聚丙烯材料,聚丙烯可以使溴水褪色
⑦科研人员积极研发抗击新型冠状病毒的疫苗,疫苗一般应冷藏存放,以避免蛋白质变性
⑧N95口罩用0.3µmNaCl颗粒进行测试,阻隔率达95%以上,戴N95口罩可有效阻隔PM2.5
⑨过氧乙酸和乙酸属于同系物
- A、 6项
- B、 5项
- C、 4项
- D、 3项
| 选项 | ① | ② | ②中实验现象和反应类型 | 实验装置 |
| A | 苯 | 溴水 | 溴水橙色褪去,液体分层。加成反应 | |
| B | 浓盐酸 | 浓硫酸 | 产生大量白雾。物理变化 | |
| C | 双氧水 | MnO2 | 产生大量气泡。分解反应 | |
| D | 浓硝酸 | 铜粉 | 产生红粽色气体。氧化还原反应 |
- A、 A
- B、 B
- C、 C
- D、 D
- A、 利用硅材料可制成光伏发电装置
- B、 SO2、漂白液、双氧水的漂白原理相同
- C、 使用无磷洗涤剂可减少水华的发生
- D、 催化净化汽车尾气可降低污染
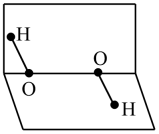
- A、 H2O2的是非极性分子
- B、 1molH2O2中含有2molσ键
- C、 H2O和H3O+的VSEPR模型不同
- D、 H2O分子之间存在氢键,因此H2O的沸点高于H2S的
实验 | 试剂a | 现象 | 结论 | |
A |
| 溶有SO2的BaCl2溶液 | 产生沉淀 | H2O2有氧化性 |
B | 酸性KMnO4溶液 | 紫色溶液褪色 | H2O2有氧化性 | |
C | KI淀粉溶液 | 溶液变蓝 | H2O2有氧化性 | |
D | 盐酸酸化的FeCl2溶液 | 溶液变黄 | H2O2有氧化性 |
- A、 A
- B、 B
- C、 C
- D、 D
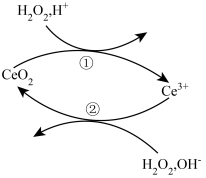
- A、 该反应历程的总反应为:H2O2=H2O+O2↑
- B、 过程①的离子方程式:2CeO2+H2O2+6H+=2Ce3++O2↑+4H2O
- C、 过程②中,每有1molCe3+参加反应时转移的电子数为3.01×1023
- D、 还原性:CeO2>H2O2
- A、 过氧乙酸能杀灭病毒的主要原因是其具有强氧化性而使病毒变性
- B、 过氧乙酸不稳定,易分解,保存时应避光,低温保存
- C、 过氧乙酸属于有机物,故属于非电解质
- D、 制备过氧乙酸时不应在金属容器中进行且不可用于金属器械的消毒
非选择题
 已知:X、A、B、C、D均为单一物质。
已知:X、A、B、C、D均为单一物质。
请回答:






