选择题
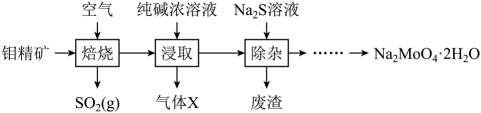
已知:浸取液溶质主要为和
。
- A、 焙烧时发生反应
- B、 气体X为
, 废渣的主要成分为
- C、 从滤液中获得
的操作为蒸发结晶
- D、 利用纯碱吸收
, 可获得副产品亚硫酸钠
- A、 原子半径Z > Y > X > R
- B、 气态氢化物的热稳定性:X > Z
- C、 R、X、Z只能组成一种共价化合物
- D、 工业上,电解熔融的氯化物制备Y的单质
①将样品加入水中,得到白色不溶物a和无色溶液
②向①中加入足量稀盐酸,产生气体,仍存在不溶物
该固体粉末一定含有的是
- A、 CaCO3、Ba( NO3)2
- B、 CaCO3、Na2SO3
- C、 Na2SO3、Ba( NO3)2
- D、 CaCO3、Na2SO3、Ba( NO3)2
菱锰矿, , 已知
,
关系如图。下列说法错误的是

- A、 “焙烧”过程
最大的是
- B、 “焙烧”过程
最大的是
- C、 “焙烧”温度应控制在
- D、 “操作X”为加热

- A、 “加热”步骤可选用水浴加热
- B、 “酸浸”产生的气体可用NaOH溶液吸收
- C、 “滤液”中溶质的主要成分为
- D、 可用盐酸和
溶液检验“滤液”中是否有

- A、 A离子中Rh原子的杂化轨道类型为
- B、 反应的总方程式为
- C、 化合物E生成
的过程为取代反应
- D、
和CO反应制备
的反应历程有2种

已知:钨酸酸性很弱,难溶于水。25℃时,和
开始沉淀的pH分别为10.3和7.3,完全沉淀的pH分别为8和5。下列说法错误的是
- A、
位于元素周期表第六周期
- B、 “系列操作”步骤仅涉及物理变化
- C、 流程中“调pH”范围为8~10.3
- D、
参与反应的化学方程式为
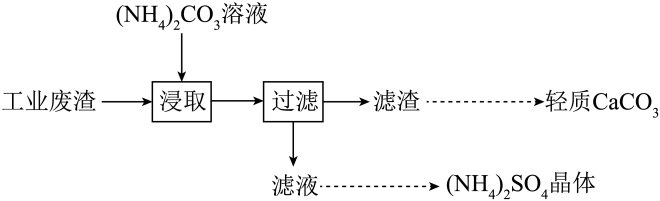
- A、 为提高浸取效率,浸取时需在高温下进行
- B、 浸取时,需向(NH4)2CO3溶液中加入适量浓氨水,抑制
水解
- C、 滤渣经洗涤和干燥后得纯净的轻质CaCO3
- D、 对滤液进行蒸发浓缩、冷却结晶可得到纯净的(NH4)2SO4晶体

- A、 b在化学反应中只能被氧化
- B、 电解饱和c溶液可得到钠单质
- C、 a→d→e的转化可以通过一步反应实现
- D、 f的阴离子空间构型为正四面体
①取少量固体加入足量水中,固体部分溶解;
②取①中滤液做焰色试验,透过蓝色钴玻璃未观察到紫色;
③取①中滤渣,向其中加入足量的盐酸,产生气泡,固体部分溶解.
下列说法错误的是
- A、 固体粉末中一定不含
- B、 固体粉末中一定含有
和
- C、 取①中滤液,加入硝酸酸化的
溶液,若未产生白色沉淀,则样品中无
- D、 为进一步确定原样品组成,可以向③未溶解的固体中加入
溶液

下列说法错误的是
- A、 “分离”时得到含硫煤油的方法是分液
- B、 “酸溶”操作的目的是除去废料中的金属氧化物
- C、 “浸取”后的分离操作所用玻璃仪器为烧杯、漏斗、玻璃棒
- D、 “酸化”时发生反应的离子方程式:
①向X中加入少量氯水,再滴加淀粉溶液,未显蓝色;
②另取100 mL X加入过量氯水,再滴加足量BaCl2(aq),得到沉淀6.99 g;
③将②反应后的混合液过滤,在滤液中加足量NaOH(aq)加热,生成0.01 mol气体。
根据上述实验,原溶液中( )
- A、 一定存在Na+、NH4+
- B、 一定存在NH4+、SO32-
- C、 一定不含Ba2+、I-
- D、 可能存在Na +、SO42-

- A、 a是一种有臭鸡蛋气味的气体
- B、 工业上由b制备e的路线:b
c
d
- C、 c造成的酸雨雨水在空气中放置一段时间pH会增大
- D、 f、g正盐的阴离子可以在碱性溶液中共存

下列说法正确的是( )
- A、 “酸化”是锆废砖粉和硫酸在硫酸铵催化作用下进行的焙烧反应,硫酸适宜用盐酸代替
- B、 “中和1”发生反应的离子方程式为Zr4+ +4OH- =Zr(OH)4 ↓
- C、 实验室模拟“焙烧”时使用的硅酸盐仪器只有烧杯和酒精灯
- D、 滤液2可以处理后返回“酸化”使用,实现循环

- A、 可代替纯碱的化学试剂有烧碱、小苏打
- B、 中和后所得滤渣主要成分是Al(OH)3、Fe(OH)3
- C、 在上述流程中得到副产品Na2SO4时需趁热过滤
- D、 母液最适宜返回酸化步骤循环利用
等产物在化工生产中都有广泛用途。在指定条件下,下列选项所示的物质间转化不能实现的是( )
- A、
- B、
- C、
- D、

- A、 “溶浸”的目的是溶解两性氧化物,除去含钙、硅的杂质
- B、 向“滤液1”中加入酸性物质使pH减小,“滤渣2”是Al(OH)3
- C、 生成Ga(OH)3的化学方程式为:2NaGaO2+3H2O+CO2=Na2CO3+2Ga(OH)3↓
- D、 工业上采用电解熔融三氧化二镓的方法制备金属镓

下列说法错误的是( )
- A、 “浸渍”时,适当提高温度,有利于提高
浸取率
- B、 滤液II中主要成分是
, 可以循环使用
- C、 “碳化”中反应的离子方程式为
- D、 已知
, 则滤液II中
沉淀完全时,
小于
多选题
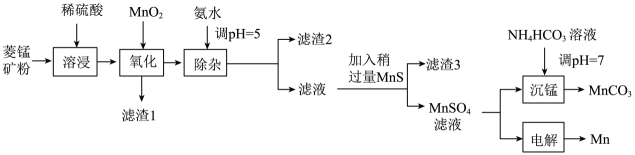
已知25℃时,部分物质的溶度积常数如表所示:
物质 | MnS | NiS | CoS | ||||
说明:整个流程中Co、Ni均为+2价。下列说法正确的是
非选择题

回答下列问题:
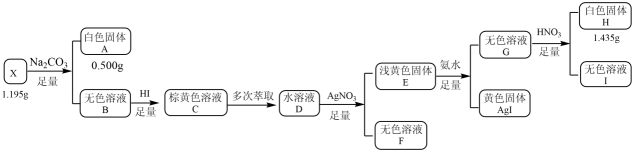
已知:白色固体A用溶解后,多余的酸用
恰好中和,请回答:

已知:①一定浓度的金属离子生成相应的氢氧化物沉淀的pH如下表所示,
| 金属氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
|
| 7.6 | 9.6 |
| | 2.2 | 3.4 |
| | 4.1 | 5.4 |
②
(无色配离子)
请回答:
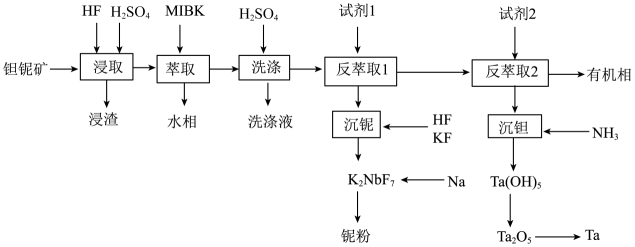
“浸取”后,浸出液中含有两种二元强酸和锰、钛等元素。
已知:①为甲基异丁基酮;②

已知几种金属阳离子的氢氧化物沉淀时的pH如下表:
金属阳离子 | ||||
开始沉淀时pH | 1.5 | 3.3 | 6.5 | 5.2 |
沉淀完全时pH | 3.7 | 5.0 | 9.7 | — |
![]()
已知:①含锌组分间的转化关系:Zn2+Zn(OH)2
②ε−Zn(OH)2是Zn(OH)2的一种晶型,39℃ 以下稳定。
请回答:

已知:①焙烧时中的Fe元素转化为
, 铝的氧化物转化为
②矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示,当溶液中可溶性组分浓度时,可认为已除尽

请回答下列问题:

已知:“焙烧”后,碲主要以TeO2形式存在,TeO2溶于强碱生成。

已知:①高温焙烧后的产物为TeO2和Cu2O;
②Cu2O在酸性条件下会发生歧化反应;
③Te元素在酸化和碱浸后分别转化为TeOSO4和Na2TeO3两种易溶于水的盐。
回答下列问题:

回答下列问题:

已知:①[Al(OH)4]-+H+ Al(OH)3+H2O,K=1013.38
②NH4VO3的溶解度( g/100g水): 0.48(20℃)、 1.32(40℃)、 2.42(60℃)
回答下列问题:

回答下列问题:




