选择题

- A、 OH-参与了该催化循环
- B、 该反应可产生清洁燃料H2
- C、 该反应可消耗温室气体CO2
- D、 该催化循环中Fe的成键数目发生变化

- A、
- B、 可计算
键能为
- C、 相同条件下,
的平衡转化率:历程Ⅱ>历程Ⅰ
- D、 历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
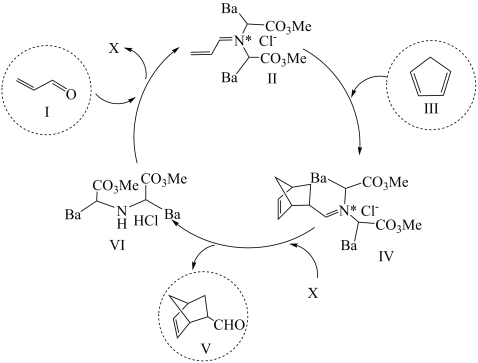
- A、 总反应为加成反应
- B、 Ⅰ和Ⅴ互为同系物
- C、 Ⅵ是反应的催化剂
- D、 化合物X为

- A、 无催化剂时,反应不能进行
- B、 与催化剂Ⅰ相比,Ⅱ使反应活化能更低
- C、 a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
- D、 使用催化剂Ⅰ时,
内,

- A、 反应原料中的原子100%转化为产物
- B、 该过程在化合物X和I-催化下完成
- C、 该过程仅涉及加成反应
- D、 若原料用
 , 则产物为
, 则产物为
| t/min | 0 | 20 | 40 | 60 | 80 |
| c/(mol·L-1) | 0.80 | 0.40 | 0.20 | 0.10 | 0.050 |
下列说法错误的是( )
- A、 反应20min时,测得O2体积为224mL(标准状况)
- B、 20~40min,消耗H2O2的平均速率为0.010mol·L-1·min-1
- C、 第30min时的瞬时速率小于第50min时的瞬时速率
- D、 H2O2分解酶或Fe2O3代替I-也可以催化H2O2分解
| 选项 | 目的 | 实验 |
| A | 制取较高浓度的次氯酸溶液 | 将Cl2通入碳酸钠溶液中 |
| B | 加快氧气的生成速率 | 在过氧化氢溶液中加入少量MnO2 |
| C | 除去乙酸乙酯中的少量乙酸 | 加入饱和碳酸钠溶液洗涤、分液 |
| D | 制备少量二氧化硫气体 | 向饱和亚硫酸钠溶液中滴加浓硫酸 |
- A、 A
- B、 B
- C、 C
- D、 D
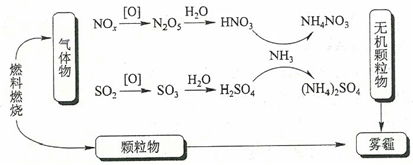
- A、 雾和霾的分散剂相同
- B、 雾霾中含有硝酸铵和硫酸铵
- C、 NH3是形成无机颗粒物的催化剂
- D、 雾霾的形成与过度施用氮肥有关
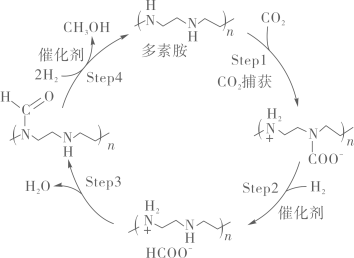
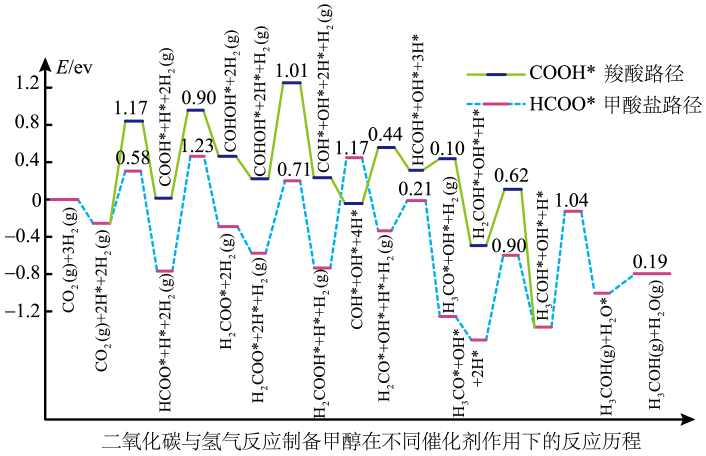
- A、 此过程总反应方程式为
- B、 产品甲醇作为重要的能源物质,可作为车用燃料
- C、 催化剂在循环过程中未参与中间反应
- D、 反应过程中既有极性键的断裂,又有非极性键的断裂

- A、 装置甲溶解固体
- B、 装置乙过滤溶液
- C、 装置丙灼烧固体
- D、 装置丁加入MnO2产生气泡速率加快
- A、 反应后所得固体除
外,还可能含有KCl、
- B、
催化
分解,降低了反应的活化能,加快分解速率
- C、 标准状况下制得22.4L氧气,反应中转移电子4mol
- D、 将制得的气体通入
溶液,可能会产生不溶于硝酸的白色沉淀

下列说法错误的是
- A、 产生1molCH3CHO转移电子数为2NA
- B、 CuCl2与PdCl2是催化剂,CuCl与Pd是中间产物
- C、 I、II、III步均发生氧化还原反应
- D、 该反应过程中既有极性键和非极性键断裂又有极性键和非极性键形成
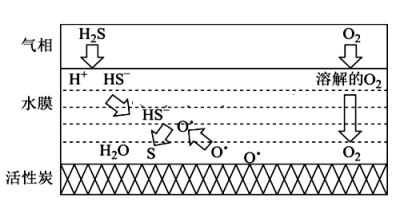
- A、 活性炭的作用为吸附剂和作催化剂的载体
- B、 温度越高,多孔炭材料催化氧化脱硫的效果越好
- C、 增加水膜的酸性会降低反应的速率
- D、 该反应的总反应方程式为:2H2S+O2=2S↓ +2H2O
多选题
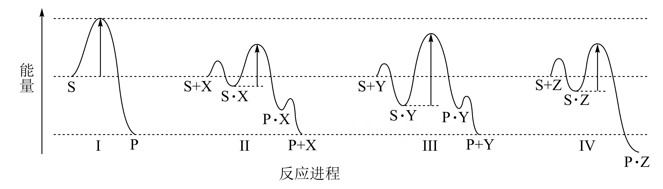
下列有关四种不同反应进程的说法正确的是( )

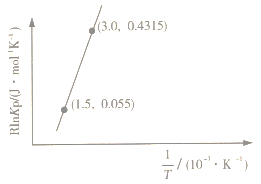
已知:RlnKp=-+C(R、C均为常数)。
下列说法错误的是( )

 )的氢烷基化反应的反应机理,下列说法错误的是
)的氢烷基化反应的反应机理,下列说法错误的是


非选择题
反应i:CO2(g)+4H2(g)CH4(g)+2H2O(g) ΔH1
反应ii:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH2=-49kJ·mol-1
CO2(g)+2H2(g)
CH4(g)+H2O(g),ΔH总Kp总 , 该反应分两步完成,反应过程如下:
①CO2(g)+H2(g)CO(g)+H2O(g),ΔH1Kp1
②CO(g)+H2(g)CO2(g)+
CH4(g),ΔH2Kp2
回答下列问题:
Ⅰ. 2H2(g)+O2(g) 2H2O(g) ΔH1= -483.6 kJ·mol-1
Ⅱ.N2(g)+O2(g) 2NO(g) ΔH2 = +180.5 kJ·mol-1
Ⅲ.2H2(g)+ 2NO(g) N2(g)+ 2H2O(g) ΔH3
(ⅰ)CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.3 kJ/mol
(ⅱ)CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.1 kJ/mol
由CO也能直接加氢合成甲醇:(iii) 2H2(g)+CO(g) CH3OH(g) △H
步骤1:向试管中加入4mL淀粉溶液,再加入少量稀硫酸,加热4分钟,冷却后将溶液分装在两支试管中;
步骤2:向一支试管中滴加几滴碘水,观察现象;
步骤3:向另一支试管中先加入烧碱溶液中和,再加入银氨溶液,水浴加热煮沸,观察现象。
下列说法错误的是( )

- A、 步骤1中加入稀硫酸可以加快淀粉水解速率
- B、 步骤2中溶液变蓝色,说明淀粉没有完全水解
- C、 步骤3中水浴加热后观察到有光亮的银镜,说明淀粉已经水解
- D、 碘晶胞如图所示,则碘分子的配位数是8
- A、 该反应在任何条件下都能自发进行
- B、 反应的平衡常数可表示为K=
- C、 使用高效的催化剂可以降低反应的焓变
- D、 其它条件不变,增大
的值,NO的转化率下降
反应I:CO(g)+2H2(g)CH3OH(g) ΔH1<0
反应II:2CO(g)+4H2(g)C2H5OH(g)+H2O(g) ΔH2<0
反应III:2CO2(g)+6H2(g)C2H5OH(g)+3H2O(g) ΔH3<0
反应IV:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH4<0
反应V:2CH3OH(g)C2H5OH(g)+H2O(g) ΔH5
回答下列问题:


 为该反应的催化剂
为该反应的催化剂

