多选题
试题详情
下列关于物质结构与性质的说法正确的是( )
试题详情
X、Y、Z、W四种短周期主族元素,原子序数依次增大,X与Z同主族,Y与W同主族;X为短周期元素中原子半径最小的元素,Y原子的最外层电子数为次外层电子数的3倍,下列说法正确的是( )
试题详情
X、Y、Z、R、W、Q为原子序数依次增大的短周期元素,其中X与W同主族,Y是形成化合物最多的元素,Q与Y同主族,W与Q同周期。已知常温下单质X与W的状态不同,R的核电荷数是Y的最外层电子数2倍,化合物QY是第三代半导体材料的典型代表。则下列推断中正确的是( )
试题详情
近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe−Sm−As−F−O组成的化合物。下列有关说法正确的是( )
试题详情
A、B、C三种元素原子的最外层电子排布分别为3s1、2s22p3和2s22p4 , 由这三种元素组成的化合物的化学式可能是( )
试题详情
德国科学家发现新配方:他使用了远古地球上存在的O2、N2、CH3、NH3、H2O和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法正确的是( )
试题详情
下列关于说法中正确的是( )
试题详情
下列离子与氖原子具有相同核外电子数的有( )
试题详情
下列分子中,所有原子都满足最外层为8电子结构的是( )
试题详情
(多选)可正确表示原子轨道的是 ( )
选择题
试题详情
阅读下列材料,完成5~7题:
周期表中IVA族元素及其化合物应用广泛。甲烷具有较大的燃烧热(890.3 kJ·mol-1),是常见燃料;Si、 Ge是重要的半导体材料,硅晶体表面SiO2能与氢氟酸(HF,弱酸)反应生成H2SiF6 (H2SiF6在水中完全电离为H+和SiF62- ); 1885年德国化学家将硫化锗(GeS2)与H2共热制得了门捷列夫预言的类硅-锗;我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜器;Pb、PbO2是铅蓄电池的电极材料,不同铅化合物一般具有不同颜色,历史上曾广泛用作颜料。
试题详情
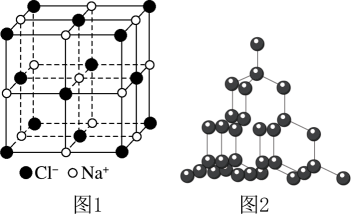
金刚石硬度大,熔点高,用途非常广泛。工业上利用反应 人工合成金刚石。已知:氯化钠晶胞结构如图1所示,相邻的
人工合成金刚石。已知:氯化钠晶胞结构如图1所示,相邻的 与
与 的距离为a cm,设
的距离为a cm,设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
- A、 Ni、Co均属于元素周期表中的d区元素
- B、
、NaCl、金刚石三种物质的熔点依次升高
- C、 若NaCl晶体密度为
, 则
- D、 12 g金刚石(晶体结构如图2所示)中含有C-C键的数目为
试题详情
氟锑酸(HSbF6)可由氢氟酸和五氟化锑反应得到,酸性是纯硫酸的2×1019倍,只能用特氟龙(即聚四氟乙烯)为材料的容器盛装。下列有关说法错误的是

- A、 基态Sb原子的简化电子排布式为[Kr]5s25p3
- B、 SbF6的VSEPR模型为正八面体
- C、 HSbF6分子中含有配位键
- D、 特氟龙号称“塑料之王”,可通过CF2=CF2加聚反应制备
试题详情
Li、Fe、Se可形成新型超导材料,晶胞如图所示(Fe原子均位于面上)。晶胞棱边夹角均为90°,X的坐标为(0,1,  ),Y的坐标为(
),Y的坐标为(  ,
,  ,
,  ),设NA为阿伏加德罗常数的值。下列说法正确的是( )
),设NA为阿伏加德罗常数的值。下列说法正确的是( )

已知:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标
- A、 基态Fe原子的核外电子排布式为[Ar]3d54s2
- B、 坐标为(
, 1,
)的原子是Li原子
- C、 Se原子X与Se原子Y之间的距离为
nm
- D、 该晶体的密度为
g·cm-3
试题详情
下列化学用语正确的是
- A、 丙烷分子的空间填充模型:

- B、 O3分子的球棍模型:

- C、 乙醇的核磁共振氢谱图:

- D、 基态As原子的电子排布式和价电子排布式分别为[Ar]3d104s24p3和4s24p3
试题详情
目前,甘肃某医药公司与北京大学共同开发研制的国家一类抗癌新药乙烷硒啉(Ethaselen)进入临床研究,其结构如图。下列说法错误的是
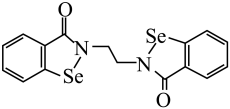
- A、 基态Se原子的核外电子排布式为
- B、 分子中有8种不同化学环境的C原子
- C、 分子中的碳原子采取
、
杂化
- D、 气态分子
的键角小于
的键角
试题详情
环碳(C18)中碳原子是单键和三键交替连接的,结构如图所示。下列说法正确的是( )
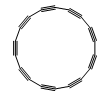
- A、 C18与C60互为同系物
- B、 12C18和14C18互为同位素
- C、 C18和金刚石互为同分异构体
- D、 环碳中碳原子均达8电子稳定结构
试题详情
六氟化硫分子(如下图)呈正八面体,难以水解,在电器工业方面有着广泛用途。下列有关SF6的推测正确的是

- A、 SF6易燃烧生成二氧化硫
- B、 SF6是极性分子
- C、 SF6中各原子均达到 8 电子稳定结构
- D、 高温条件下,SF6微弱水解生成H2SO4和HF
非选择题
试题详情
硅材料在生活中占有重要地位。请回答:
试题详情
工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为: 。回答下列问题:
。回答下列问题:
试题详情
1962年首个稀有气体化合物 问世,目前已知的稀有气体化合物中,含氙(54Xe)的最多,氪 (36Kr)次之,氩(18Ar)化合物极少。
问世,目前已知的稀有气体化合物中,含氙(54Xe)的最多,氪 (36Kr)次之,氩(18Ar)化合物极少。 是
是 与
与 分子形成的加合物,其晶胞如下图所示。
分子形成的加合物,其晶胞如下图所示。

回答下列问题:
试题详情
【选修3:物质结构与性质】
含Cu、Zn、Sn及S的四元半导体化合物(简写为CZTS),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
试题详情
铁(Fe)、钴(Co)、镍(Ni)是第四周期第Ⅶ族的元素,其化合物在生产生活中应用广泛。
试题详情
铁及其化合物在生活、生产中有重要应用。回答下列问题:
试题详情
碳的多种同素异形体及一系列化合物广泛应用于科研、医疗、工农业生产等领域。回答下列问题:
试题详情
邻羟基苯甲酸俗称水杨酸,具有抗炎、抗菌、角质调节等作用。其分子结构如图所示。

试题详情
钕铁硼磁铁在绝对零度时磁性仅次于钬磁铁,但是在常温下磁性远远强于目前已知的所有永久磁铁。生产钕铁硼磁铁的主要原料有稀土金属钕、纯铁、铝硼及其他稀土原料。
试题详情  是一种锂离子电池的正极材料,放电时生成
是一种锂离子电池的正极材料,放电时生成 。
。
试题详情
LiFePO4常用作车载动力电池的正极材料。以碳酸锂、草酸亚铁,磷酸二氢铵为主要原料经高温锻烧可制备LiFePO4。
试题详情
铁、硒、铜都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
试题详情
配合物是近代无机化学的重要研究对象,Cu或Cu2+常作为中心原子或离子,H2O、CN-、吡啶(C5H5N)等粒子是常见的配体。
试题详情
中国古代艺术作品色彩艳丽,璀璨夺目,离不开矿物颜料的使用。请回答下列问题:




