
 + H218O
+ H218O 
①电负性由大到小的顺序是。
②原子半径由大到小的顺序是。
③在元素周期表中的分区与其他两种不同的是。
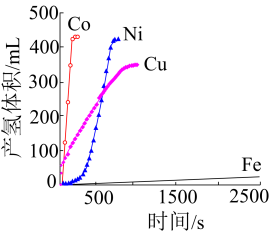
这四种催化剂中:
①催化效果最好的金属基态原子中未成对的电子数为。
②催化效果最差的金属基态原子的价层电子排布式为。

已知:①xNH4Cl·yScF3·zH2O是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
②“脱水除铵”是复盐沉淀的热分解过程。
③25℃时,部分物质的相关信息如表所示:
Ksp(PbSO4) | Ksp(PbC2O4) | Ka1(H2C2O4) | Ka2(H2C2O4) |
2.0×10-8 | 5.0×10-10 | 6.0×10-2 | 6.25×10-5 |


已知:①3Cl2+6NaOH5NaCl+NaClO3+3H2O
②2NaClO+(CNO)3H3=(CNO) 3Cl2Na+NaOH+H2O
回答下列问题:
反应原理:
[(CNO)3Cl2]-+H++2H2O=(CNO)3H3+2HClO
HClO+2I-+H+=I2+Cl-+H2O
I2+2S2O=S4O
+2I-
实验步骤:准确称取wg样品配成100mL溶液,取25.00mL于碘量瓶中,加入适量稀硫酸和过量KI溶液,暗处静置充分反应后,用0.1000 mol·L-1Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液VmL。
①滴定终点的现象是。
②该样品中有效氯含量的表达式为。(有效氯=100%)。
③若滴定前滴定管尖嘴有气泡,滴定后气泡消失,则有效氯的测定值将(填“偏高”、“偏低”或“无影响”)。

①
②
③
④
其中控速步骤为(填方程式代号),用合适的微粒符号补全反应②;

①A点坐标为(t,);
②的平衡转化率为。
③反应的平衡常数
。