 B .
B .  C .
C .  D .
D . 
| | | | |
| A.制CO2的药品 | B.发生装置 | C.收集装置 | D.比较CO2与空气的密度 |

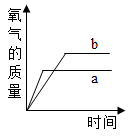 B .
B . 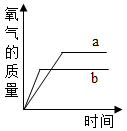 C .
C . 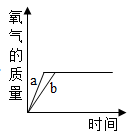 D .
D . 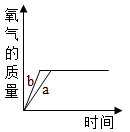


①“箭头”画出了“氧气”应行走的路线,“氧气”不能从甲处通过,你认为甲处放的物质是(填字母)。
A.硫 B.水 C.氦气
②氧气在进迷宫过程中,碰到了三种阻止它前进的物质,请写出氧气与铁点燃条件下发生反 应的方程式:;这三个反应都会(选填“放热”或“吸热”)。
友情提示:使用分液漏斗时,可通过开启、关闭活塞控制液体的流入,同时防止装置漏气;浓硫酸能干燥气体,不与二氧化碳反应;二氧化碳与氢氧化钠反应无现象,原理与二氧化碳和氢氧化钙反应类似。
