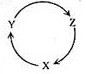
| 选项 | X | Y | Z |
| A | Na | NaOH | NaHCO3 |
| B | Cu | CuSO4 | Cu(OH)2 |
| C | C | CO | CO2 |
| D | Si | SiO2 | H2SiO3 |

| 实验序号 | 实验操作 | 实验现象 |
| 1 | 将FeCl3溶液加热片刻 | 溶液颜色变深 |
| 2 | 向FeCl3 溶液中通入少量HCl气体 | 溶液颜色变浅 |
| 3 | 向FeCl3溶液中加入少量(NH4)2SO4固体 | 溶液颜色变浅 |
| 4 | 向FeCl3溶液中加入少量NaHCO3固体 | 产生红褐色沉淀,溶液中出现大量气泡 |
下列有关说法正确的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 配制100mL1.0mol/LCuSO4溶液 | 将25g CuSO4·5H2O溶于100mL蒸馏水中 |
| B | 除去CuO中混有的Al2O3 | 加入过量NaOH溶液后,过滤、洗涤、干燥 |
| C | 证明氧化性:H2O2>Fe3+ | 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 |
| D | 证明非金属性:Cl>C | 向NaHCO3溶液中加入过量盐酸振荡、静置、观察 |
| 选项 | 实验目的 | 实验方案 |
| A | 除去苯中混有的苯酚 | 加入适量的溴水充分反应后过滤 |
| B | 检验Fe2+溶液中是否含有Fe3+ | 向待测液中滴加几滴铁氰化钾溶液 |
| C | 除去粗盐中含有Mg2+、Ca2+、SO42-的试剂加入顺序 | 向该溶液中先加入NaOH溶液、再加BaCl2溶液,最后加碳酸钠溶液 |
| D | 检验SO2中是否含有HCl | 将产生的气体通入HNO3酸化的AgNO3溶液中 |
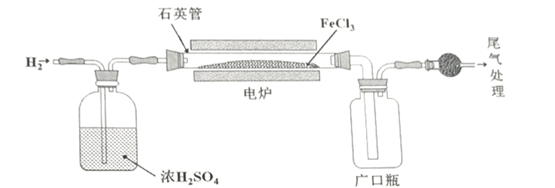
已知有关物质的性质如下:
| FeCl3 | FeCl2 | Fe | |
| 熔点/℃ | 升华,易水解 | 672 | 1538 |
| 沸点/℃ | 1023 | 2750 |
①当温度T为300℃时,加热一段时间后发现石英管内几乎没有固体剩余,请指出出现该现象可能的原因:。
②当温度T为 330℃时,加热后石英管内有固体剩余,取少量固体于试管中并加入稀盐酸,全部溶解且无气泡,对固体成分进行猜测并设计实验验证。
猜测1:只有 FeCl2;猜测2: 含有FeCl2和 FeCl3;猜测3: 只有FeCl3
实验方案:
|
实验步骤 |
操作 |
现象 |
|
第一步 |
取溶液2mL于试管中,加入KSCN |
现象一 |
|
第二步 |
另取溶液2mL于试管中,加入 |
现象二 |
第二步加入的物质为:。
实验结论:现象一为,现象二为。则猜测1 成立。
③当温度T为350℃时,加热后石英管内有固体剩余,取少量固体于试管中并加入稀盐酸,固体溶解的同时有少量气泡产生,写出加热过程中发生的副反应的化学方程式:。
Ⅰ.某实验小组分别用水煮检验法和灼烧检验法对菠菜中的铁元素(主要以难溶的 形式存在)进行检测。实验如下:
a.水煮检验法:

b.灼烧检验法:
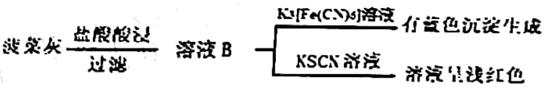

已知:几种物质的溶解度( )如下:
| | | | |
| 20℃ | 48 | 75 | 37 |
| 60℃ | 101 | 88 | 38 |
趁热过滤的原因是:。
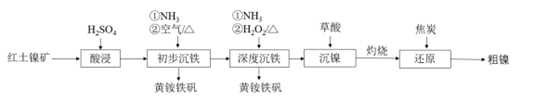
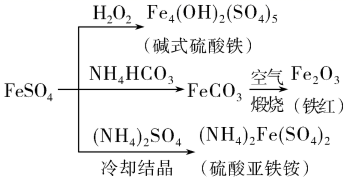
①溶液中Fe3+转化为黄铵铁矾的离子方程式为。
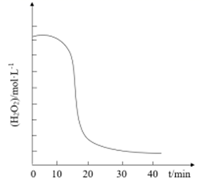
②溶液中c(H2O2)随时间t的变化关系如图所示,反应开始10~20 min内c(H2O2)迅速减小,其原因是。
|
金属离子的氢氧化物 |
Ni(OH)2 |
Fe(OH)3 |
黄铵铁矾 |
|
开始沉淀pH |
7.1 |
2.7 |
1.3 |
|
沉淀完全pH |
9.2 |
3.7 |
2.3 |
“深度沉铁”中通入NH3调节溶液pH的范围是。
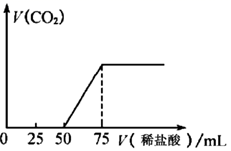
请回答下列问题
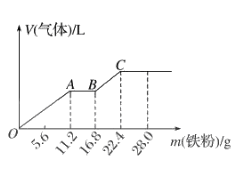
①通入二氧化碳后形成溶液的溶质成分是(填写化学式)
②滴入 稀盐酸过程中,溶液导电性(填“增强”或“减弱”),试解释其原因。
③原 氢氧化钠溶液的浓度为。
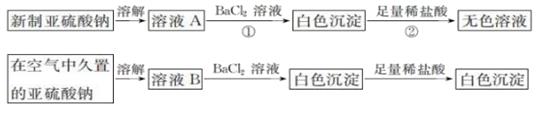
写出上述实验中②的离子方程式:。
①中反应的离子方程式是._。
甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液, 产生白色沉淀。得出结论:
FeCl3与Na2SO3 发生了氧化还原反应,离子方程式是_。
乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是_。
回答下列问题:
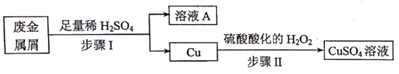
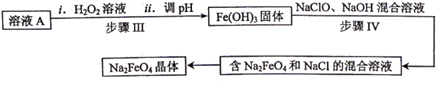
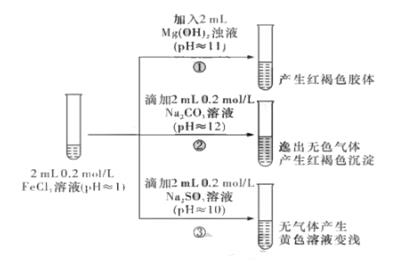
写出步骤Ⅳ中反应的离子方程式。
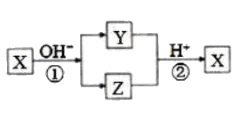
①若试剂1和试剂2的酸碱性相同,则C溶液显(填“酸性”、“碱性”或“中性”);
②若试剂1和试剂2的酸碱性不同,试剂1和B的离子方程式是。
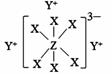
①Y单质与稀硝酸反应生成E时,Y单质必须过量,写出该反应的离子方程式。如果稀硝酸过量,则会有Fe3+生成,可以选择试剂 进行验证。
②D的阳离子检验可以用试剂 检验。