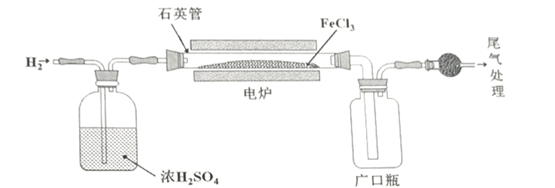
已知有关物质的性质如下:
| FeCl3 | FeCl2 | Fe | |
| 熔点/℃ | 升华,易水解 | 672 | 1538 |
| 沸点/℃ | 1023 | 2750 |
①当温度T为300℃时,加热一段时间后发现石英管内几乎没有固体剩余,请指出出现该现象可能的原因:。
②当温度T为 330℃时,加热后石英管内有固体剩余,取少量固体于试管中并加入稀盐酸,全部溶解且无气泡,对固体成分进行猜测并设计实验验证。
猜测1:只有 FeCl2;猜测2: 含有FeCl2和 FeCl3;猜测3: 只有FeCl3
实验方案:
|
实验步骤 |
操作 |
现象 |
|
第一步 |
取溶液2mL于试管中,加入KSCN |
现象一 |
|
第二步 |
另取溶液2mL于试管中,加入 |
现象二 |
第二步加入的物质为:。
实验结论:现象一为,现象二为。则猜测1 成立。
③当温度T为350℃时,加热后石英管内有固体剩余,取少量固体于试管中并加入稀盐酸,固体溶解的同时有少量气泡产生,写出加热过程中发生的副反应的化学方程式:。