选择题(本大题共15小题,每小题3分,共45分,在每小题给出的四个选项中,只有一项是符合题目要求的)
试题详情
下列说法正确的是( )
- A、 已知
, 该反应为熵减小的反应
- B、 氢氧化钠固体溶于水体系温度升高,是因为发生了放热反应
- C、 甲烷燃烧放热,是因为破坏反应物化学键所需的能量特别大
- D、 已知乙醚的摩尔燃烧焓为
, 则表示乙醚摩尔燃烧焓的热化学方程式为:
,
试题详情
已知植物光合作用发生的反应如下: ,
,  该反应达到化学平衡后,下列说法正确的是( )
该反应达到化学平衡后,下列说法正确的是( )
- A、 取走一半
,
转化率增大
- B、 适当升高温度,既提高了反应速率,又增大了
的转化率增大
- C、 加入催化剂,
的体积分数增大
- D、 增大
的浓度,平衡右移,化学平衡常数增大
试题详情
关于中和热测定的实验,下列说法正确的是( )
- A、 可以使用铜质搅拌器代替玻璃搅拌器
- B、 用温度计测量盐酸溶液温度后,直接测量
溶液温度
- C、 为了防止倾倒时液体溅出,应该沿内筒的内壁缓慢倾倒
溶液
- D、 计算温度差时,若实验中某次数据偏差较大,应舍去
试题详情
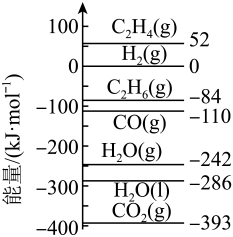
已知热化学方程式 ,
,  , 则下列说法正确的是( )
, 则下列说法正确的是( )
- A、 降低温度,平衡正向移动,方程式中的a值增大
- B、 将
置于一密闭容器中充分反应,需吸收akJ的热量
- C、
、
分子中的键能总和大于
分子中的键能
- D、 若参加反应的
数目为
, 反应会吸收akJ热量
试题详情
蓄电池是一种可以反复充电、放电的装置。某蓄电池在充电和放电时发生的反应是: , 下列有关该电池的说法正确的是( )
, 下列有关该电池的说法正确的是( )
- A、 充电时,
发生氧化反应
- B、 放电时可将化学能完全转化为电能
- C、 放电时,
移向该电池的正极
- D、 充电时,Fe电极为阳极,电极反应式为:
试题详情
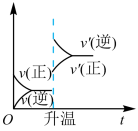
化学反应有多种理论,图1为有效碰撞理论,图2为使用催化剂和不使用催化剂时能量变化的过渡态理论。下列说法错误的是( )

- A、 图1中Z表示有效碰撞
- B、 通过图1可知:有效碰撞时反应物分子要有合适的取向
- C、 图2中虚线代表有催化剂时的反应过程
- D、 通过图2可知:催化剂能改变反应的焓变
试题详情
2016年7月美国康奈尔大学的研究人员瓦迪·阿尔·萨达特和林登·阿彻在发表于《科学进展》(ScienceAdvances)上的一篇论文中,描述了一种能够捕捉二氧化碳的电化学电池的设计方案。其简易结构如下图。下列说法错误的是( )
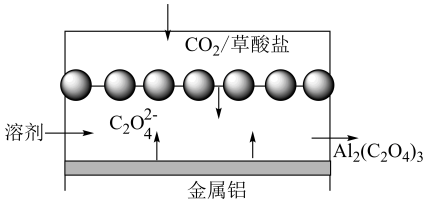
- A、 金属铝作为还原剂参与负极的氧化反应
- B、 该装置除了吸收
之外还可得到化工产品
- C、 该装置每消耗27kg的金属铝,可以吸收
- D、 该装置的正极反应方程式为:
试题详情
硫化氢( )是一种有毒气体,对环境和人体健康造成极大的危害。工业上采用多种方法减少
)是一种有毒气体,对环境和人体健康造成极大的危害。工业上采用多种方法减少 的排放。生物脱
的排放。生物脱 的原理为:
的原理为:
① ,
② ,
下列说法不正确的是( )

- A、 已知硫杆菌存在时,
被氧化的速率是无菌时的
倍,则该菌起催化作用
- B、 由图甲和图乙判断使用硫杆菌的最佳条件是
、
- C、
是反应②的反应物,
越大反应速率越快
- D、 生物脱
的总反应为:
试题详情
在微生物参与下,采用惰性电极处理污水中有机物的某微生物燃料电池原理如图。下列说法正确的是( )
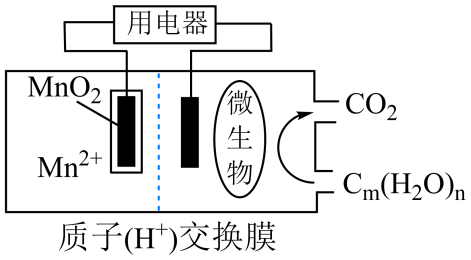
- A、 升高温度可提高电池的能量转化效率
- B、 电池正极反应式为:
- C、 有机物在微生物作用下被氧化并释放质子
- D、 若有机物为葡萄糖(
),则1mol葡萄糖被完全氧化时,理论上转移
试题详情
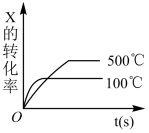
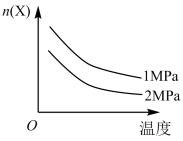
工业制备粗硅的过程中,有一步反应为: , 其转化率随温度变化如图所示。下列说法正确的是( )
, 其转化率随温度变化如图所示。下列说法正确的是( )

- A、 该反应为吸热反应
- B、 加压有利于提高
的转化率
- C、 q点
- D、 O点前,转化率升高的原因可能是升高温度平衡正向移动造成的
试题详情
我国正在研究利用甲烷合成甲醇这种清洁能源,反应原理为:

 , 100℃时,将一定量的
, 100℃时,将一定量的 和一定量
和一定量 通入10L恒容容器中,若改变起始量,
通入10L恒容容器中,若改变起始量, 的平衡转化率如表所示:
的平衡转化率如表所示:
甲 | 乙 | 丙 | ||
起始物质的量 | 5 | 4 | 10 | |
10 | 8 | 10 | ||
| ||||
下列说法不正确的是( )
- A、 按甲投料反应达到平衡所需的时间为5min,则用甲烷表示0~5min内的平均反应速率为
- B、 增大
可提高
转化率且不改变该反应的平衡常数
- C、 在不改变其他外界条件下
、
、
的相对大小顺序为:
- D、
比值增大,可提高甲烷转化率,平衡常数不变
试题详情  时,向容积为
时,向容积为 的密闭容器中充入一定量的
的密闭容器中充入一定量的 和
和 , 发生如下反应:
, 发生如下反应: , 反应过程中测定的数据见下表(表中
, 反应过程中测定的数据见下表(表中 )。
)。
反应时间/ | ||||
0 | 1.80 | 0.90 | 0 | 0 |
1.20 | ||||
0.60 |
下列说法正确的是( )
- A、
时反应没有达到平衡状态
- B、 容器内的压强不变,可说明反应达到平衡状态
- C、 若初始量
:
、
:
, 则平衡时
- D、 若初始量
和
均为
, 此时反应已经处于平衡状态
试题详情
相同金属在其不同浓度盐溶液中可形成浓差电池。科学家利用浓差电池采用电渗析法提纯乳清(富含NaCl的蛋白质),有价值的蛋白质的回收率达到98%,工作原理如图所示(a、b电极均为石墨电极)。
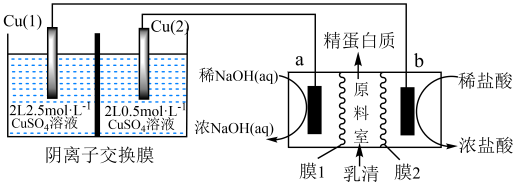
下列说法正确的是( )
- A、 电池从开始工作到停止放电,电解池理论上可制得
- B、 膜1为阴离子交换膜,膜2为阳离子交换膜
- C、 电池放电过程中,
电极上的电极反应为
- D、 每转移1mol电子,理论上乳清质量减少29.25g