选择题(本大题共14小题,每小题3分,满分42分,每小题只有一个选项符合题意。)
试题详情
化学与生活、生产、环境息息相关。下列叙述错误的是( )
- A、 食物放入冰箱中冷藏,其目的是减慢化学反应速率
- B、 选择合适的催化剂可有效减少汽车尾气中有害气体的排放
- C、 打开汽水瓶盖时有大量气泡冒出,该现象能用勒夏特列原理解释
- D、 煤的气化,有利于提供更多的能量,同时有效地减少温室气体的产生
试题详情
下列叙述正确的是( )
- A、 NaClO属于弱电解质
- B、 正丁烷
异丁烷
, 正丁烷相对稳定
- C、 测量中和反应反应热的实验中,每次平行实验至少需要记录3次温度
- D、 根据
是吸热反应,推测
也是吸热反应
试题详情
对
 反应,下列观点正确的是( )
反应,下列观点正确的是( )
- A、 1 mol
的总能量一定小于1 mol
和1 mol
的总能量
- B、 升高温度,
减小、
增大
- C、 增加C粉用量能加快反应速率
- D、 升高温度和增大压强均可增大活化分子百分数
试题详情
工业合成氨生产中,为了提高原料气总平衡转化率,采取的措施正确的有( )
①增大压强;②选择高效催化剂;③及时分离出氨气;④将反应混合物中分离出的氢气和氮气进行循环操作
- A、 ③④
- B、 ①②③
- C、 ①③④
- D、 ①②③④
试题详情
有研究认为,强碱性溶液中反应 分三步进行,其中两步如下:
分三步进行,其中两步如下:
第ⅰ步:
第ⅱ步:
下列说法正确的是( )
- A、 第ⅰ步反应能说明
具有氧化性
- B、 第ⅲ步反应为
- C、 第ⅰ步反应
表达式为
- D、 第ⅰ步反应为中和反应的逆反应,故
比较大
试题详情
将一定量纯净的氨基甲酸铵置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在绝热条件下使其达到分解平衡: 。能判断该反应已经达到化学平衡状态的是( )
。能判断该反应已经达到化学平衡状态的是( )
①
②密闭容器中温度不变
③密闭容器中混合气体的密度不变
④断裂3 mol N-H键的同时形成1 mol 键
⑤密闭容器混合气体的总物质的量不变
⑥混合气体总质量不变
⑦密闭容器中的体积分数不变
- A、 ①②③⑤⑦
- B、 ②③④⑤⑥
- C、 ①③④⑤⑥
- D、 ②④⑤⑥⑦
试题详情
已知:各相关物质的燃烧热数据,如下表。
物质 | |||
燃烧热 | -393.5 | -1366.8 | -285.8 |
下列热化学方程式正确的是( )
- A、
kJ⋅mol
- B、
kJ⋅mol
- C、
kJ⋅mol
- D、
kJ⋅mol
试题详情
恒温恒容条件下,反应 分两步进行,
分两步进行,
①、②
的能量-反应过程图如下所示。
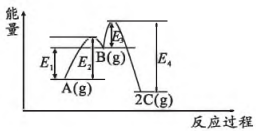
下列有关该反应的叙述正确的是( )
- A、 加入催化剂,
减小
- B、 总反应的能量变化为
- C、 起始
越大,A的转化率越高
- D、 反应②在升高温度时,平衡向逆反应方向移动
试题详情
用酸性高锰酸钾溶液与草酸( )溶液反应来探究浓度和温度对反应速率的影响(假设溶液体积可以加和),设计的实验方案和得到的速率图像如下,下列说法错误的是( )
)溶液反应来探究浓度和温度对反应速率的影响(假设溶液体积可以加和),设计的实验方案和得到的速率图像如下,下列说法错误的是( )
实验编号 | 室温下,试管中所加试剂及其用量/mL | 实验温度/℃ | 溶液颜色褪至无色所需时间/min | |||
0.6 mol·L | 3 mol·L | 0.05 mol·L | ||||
Ⅰ | 2.0 | 2.0 | 3.0 | 20 | 2.6 | |
Ⅱ | 2.0 | 2.0 | 3.0 | T | 1.4 | |
Ⅲ | 2.0 | 3.0 | 2.0 | 3.0 | 45 | 1.0 |
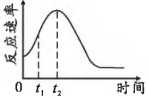
- A、 某同学认为也可以通过改变
溶液的浓度探究浓度变化对速率的影响
- B、
后反应速率逐渐减小的原因是浓度变化对速率的影响为主要因素
- C、 实验Ⅲ中,从反应开始至
溶液褪至无色时间段内,
mol⋅L
⋅min
- D、
试题详情
已知:亚硝酸( )是一种弱酸,亚硝酸钠(
)是一种弱酸,亚硝酸钠( )是一种常用的食品防腐剂。常温下,将0.1 mol⋅L
)是一种常用的食品防腐剂。常温下,将0.1 mol⋅L
 溶液加水稀释或加入少量
溶液加水稀释或加入少量 晶体时,下列观点正确的是( )
晶体时,下列观点正确的是( )
- A、 加水稀释时,电离平衡正向移动,溶液中
增大
- B、 加
晶体时,电离平衡逆向移动,溶液导电能力增强
- C、 加水稀释时,
的电离程度增大,电离常数也增大
- D、 加
晶体时,溶液的pH增大,与
增大有关
试题详情
下列实验方案设计、现象和结论都正确的是( )
选项 | 目的 | 方案设计和现象 | 结论 |
A | 证明 | 用pH计分别测量醋酸溶液和盐酸的pH,醋酸溶液的pH大 |
|
B | 探究压强对化学平衡的影响 | 先将注射器充满 | 加压,平衡向生成 |
C | 探究浓度对化学平衡的影响 | 向 | 增大 |
D | 比较 | 向两份等浓度、等体积且等温的过氧化氢溶液中分别加入2滴等浓度的 | 催化效率: |
- A、 A
- B、 B
- C、 C
- D、 D
试题详情
25℃,将10 mL溶液中 均相同HA、HB的两种溶液,加水稀释至1000 mL,溶液中
均相同HA、HB的两种溶液,加水稀释至1000 mL,溶液中 随溶液体积的变化如图所示:
随溶液体积的变化如图所示:
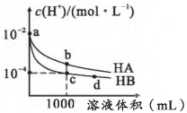
下列判断正确的是( )
- A、 HB是弱电解质
- B、 中和NaOH的能力:c>d
- C、 该条件下能计算出电离平衡常数
- D、 a点溶液:
、b点溶液
点溶液
试题详情
向甲、乙、丙三个恒温密闭容器中充入一定量的A和B,发生反应(x为正整数):
 kJ⋅mol
kJ⋅mol (
( ),各容器的容积、反应温度、反应物起始量如表所示,
),各容器的容积、反应温度、反应物起始量如表所示,
容器 | 甲 | 乙 | 丙 |
容积 | 1 L | 1 L | 1 L |
温度/℃ | |||
反应物 起始量 | 3 mol A 1 mol B | 3 mol A 1 mol B | 6 mol A 2 mol B |
其中甲、丙容器反应过程中C的浓度随时间变化关系如图所示:
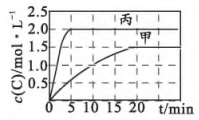
下列分析与推断错误的是( )
- A、
- B、 不能判断
、
相对大小
- C、 平衡时乙容器中
mol⋅L
- D、 该反应在
℃下的化学平衡常数



