1.
(2021九上·萧山月考)
牙膏常用碳酸钙、二氧化硅等物质作为摩擦剂,某同学对摩擦剂中碳酸钙的含量进行探究.
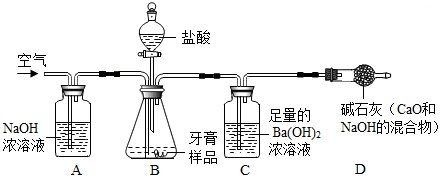
实验原理:测定下图C装置中生成的BaCO3沉淀的质量,通过计算确定牙膏中CaCO3的质量分数。
查阅资料:①CO2+Ba(OH)2=BaCO3↓+H2O,牙膏中其他成分遇到盐酸时无气体产生;
②饱和碳酸氢钠可以吸收HCl气体,且发生反应的化学方程式为NaHCO3+HCl=NaCl+H2O+CO2;
③CO2不会溶于饱和碳酸氢钠溶液。实验装置如下图根据探究过程回答下列问题:
-
(1)
从C中过滤出BaCO3沉淀所需的玻璃仪器有烧杯、玻璃棒和。
-
-
(2)
实验过程中先后两次鼓入空气,其中第二次鼓入空气的目的是:。
-
-
(3)
实验中准确称取4g样品三份,进行三次测定,测得BaCO3平均质量为1.97g,则样品中碳酸钙的质量分数为。
-
-
(4)
下列各项措施中,不能提高测定准确度的是______(填字母)。
A . 滴加盐酸不宜过快
B . 在加入盐酸之前,应排尽装置内的CO2气体
C . 在A—B之间增添盛有浓硫酸的洗气装置
D . 在B—C之间增添盛有饱和碳酸氢钠溶液的洗气装置
E . 滤出的BaCO3沉淀应该洗涤、干燥后再称质量。
-
