将用砂纸打磨过的在空气中燃烧,生成
和
, 氮化镁溶于水得到
固体和
, 将
固体溶于
, 得到无色溶液,将无色溶液经过一系列操作得到
, 将
在
气流中加热得到
。
实验2:将已经打磨过的、大小相同的镁条与铝片分别同时投入足量的稀硫酸中,相同时间内,观察到的现象为,可得出的结论是。
的部分性质如下表:
物理性质 | 常温下,具有强烈刺激性气味的黄棕色气体:熔点: |
化学性质 |
|
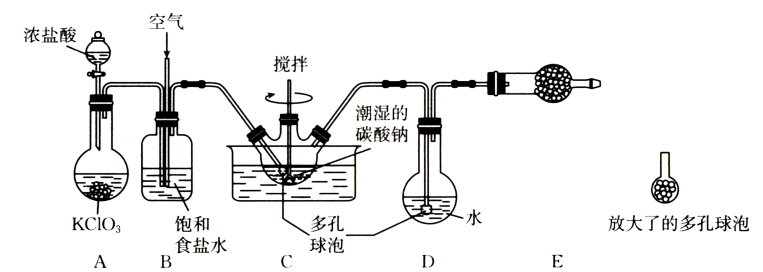
A. B.
C.
请回答下列问题:
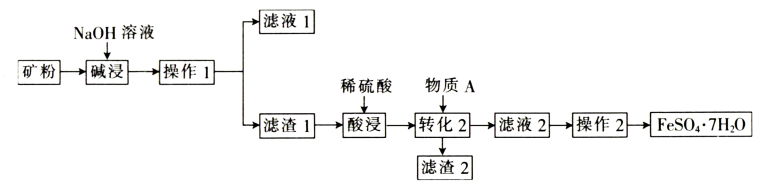
请回答下列问题:
①若配制样品溶液的过程中,容量瓶中有少量蒸馏水残留,则对所配溶液浓度的影响是(填“偏低”“偏高”或“无影响”)。
②样品的纯度约为(保留三位有效数字)。