①量取浓时,适宜的量筒规格为(填标号)。
A.10mL B.25mL C.50mL D.100mL
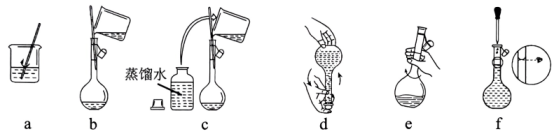
②配制溶液时,进行如下操作:
溶解→冷却→操作ⅰ→洗涤→注入→混匀→定容→操作ⅱ→装瓶贴标签下图、(填标号)所示操作依次为操作ⅰ、操作ⅱ。
在20℃、101kPa下,电流为0.2A,以精铜片为电极,电解溶液,10min后关闭电源。观察和测量结果如下:
a.阳极上有少量气泡产生,且铜片质量减少mg;
b.阴极上有大量气泡产生;
c.电解质溶液变蓝。
①为准确测量,电解前需将已除去油污的铜片,并用蒸馏水洗净擦干后再称重。
②经检验,阳极上产生的气体为 , 电极反应为;该副反应的发生,可能导致
的测定值比其理论值(填“偏大”或“偏小”)。
查阅资料:电解过程中,电解电压低将导致反应速率慢,电压高则易引发电极副反应。电流强度相同时,电压与电解质溶液的浓度成反比。
提出猜想:猜想ⅰ:电流强度越大,越容易引发电极副反应。
猜想ⅱ:硫酸浓度越低,越容易引发电极副反应。
进行实验:其他条件相同时,进行如下表实验,利用电流传感器测定通过电路的电量Q , 并测算3min内阳极铜片质量的减少量。
实验编号 | 理论电流I/A | 实测电量Q/C |
| 蒸馏水的体积/mL | 阳极铜片减少的质量/g |
1 | 0.1 | 18.33 | a | 0 | 0.0060 |
2 | 0.1 | 18.34 | 20 | 180 | 0.0055 |
3 | 0.2 | 36.70 | b | c | 0.0095 |
4 | 0.3 | 55.02 | 20 | 180 | 0.0130 |
①根据表中信息,补充数据:a=,b=。
②由实验2、3和4可知,猜想ⅰ成立,结合表中数据,给出判断理由:。
③根据实验1~4相关数据,由实验(填实验编号)测算的值误差最小。
实验结论:
④根据最优实验条件的数据计算,(已知:
)。

已知:
①“酸溶”后溶液中各金属元素的存在形式为:、
、
、
;
②25℃时, ,
;
③部分易升华物质在接近沸点时升华速率较快。“加氢还原”前后相关物质沸点如下:
物质 | |||||
沸点/℃ | 331 | 315 | 1300 | 700 | 1150 |
回答下列问题:
②沸点远低于
的可能原因为。
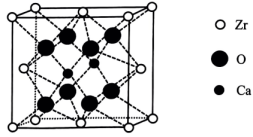
①晶体中每个O周围与其最近的O个数为。
②已知该晶胞为立方晶胞,晶胞中O与Zr的最小间距为anm,设为阿伏加德罗常数的值,该晶体的密度为
(列出计算式)。
③如图所示结构(![]() -Zr
-Zr ![]() -O
-O ![]() -Ca)与上述晶胞结构不一致的是(填标号)。
-Ca)与上述晶胞结构不一致的是(填标号)。
A.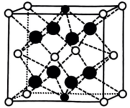 B.
B.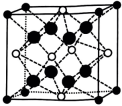
C. D.
D.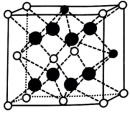
(ⅰ)
(ⅱ)
(ⅲ)
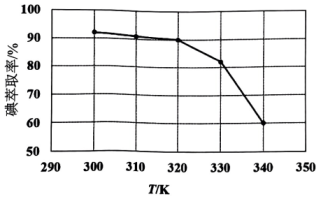
萃取温度从300K升高至320K,碘萃取率缓慢下降。结合平衡移动原理,分析其原因(忽略萃取剂的挥发、的挥发及
分解产生的影响)。当萃取温度超过320K时,
的分解导致碘萃取率明显下降。
②下列说法不正确的是(填标号)。
A.增大溶液的pH,碘萃取率降低 B.增大萃取剂用量,碘萃取率升高
C.萃取体系平衡后加水稀释,变小 D.增大
的浓度,反应(ⅰ)的速率增大
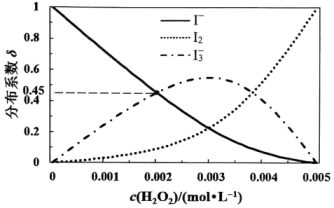
①设平衡时、
、
分别为
、
、
, 则a、b、c之间的关系式为=0.01。
②计算反应的平衡常数
(结果保留3位有效数字)。

序号 | 反应试剂、条件 | 反应形成的新结构 | 反应类型 |
a |
| ||
b | 浓 | 消去反应 |
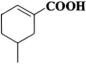 的路线(不用注明反应条件)。
的路线(不用注明反应条件)。