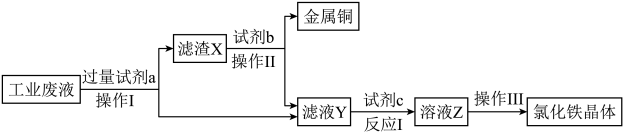
回答下列问题:
A.Zn B.H2O2 C.NaOH D.稀H2SO4
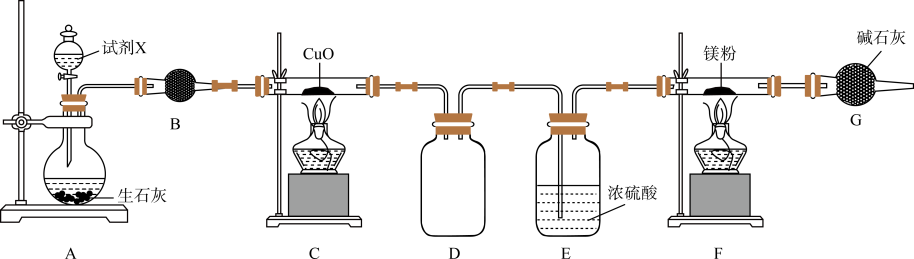
已知:NH3具有还原性,在加热时可将CuO还原成Cu。回答下列问题:
a.五氧化二磷 b.无水氯化钙 c.碱石灰 d.活性炭
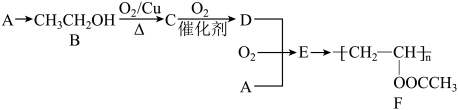
已知:烃A是石油裂解气的主要成分之一,相同状况下,烃A相对于H2的密度为14。
回答下列问题:
①与B互为同系物
②相对分子质量比B大28
其中一种的结构简式为。
a.F为纯净物
b.A、B都能使酸性KMnO4溶液褪色
c.可用大理石鉴别B、D两种物质的水溶液
d.向装有B的试管中投入一小粒钠,钠浮于液面上