Ⅰ.某实验小组设计了如图在纽扣上电镀铜的实验装置:
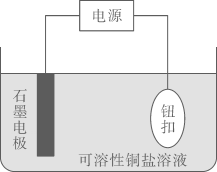
装置示意图 | 序号 | 电解质溶液 | 实验现象 |
| ① | 0.1mol/L | 阴极表面有无色气体,一段时间后阴极表面有红色固体,气体减少。经检验,铁电极表面有 |
② | 0.1mol/L | 阴极表面未观察到气体,一段时间后阴极表面有致密红色固体,经检验,电解液中无Fe元素。 |
实验①中,无色气体产生的原因是或。


①由图可知,溶液减小,
的平衡转化率(填“增大”“减小”或“不变”)。根据A点数据,计算出反应A的平衡常数为。
②升高温度,溶液中的平衡转化率减小;则反应A的
(填“>”或“<”)0。
③向酸性溶液中加水,有同学认为溶液中所有离子的浓度都减小,你是否同意并说明理由。
④向酸性溶液(橙色)中加入少量氢氧化钠固体(忽略溶液体积的变化),振荡后立即观察到溶液变为黄色,该结果不足以证明
浓度的减小使得反应A的平衡逆向移动,理由是:。