t/ min | 0 | 5 | 10 | 15 | 20 |
n/ mol | 0 | 0.3 | 0.5 | 0.6 | 0.6 |
下列叙述正确的是

下列叙述错误的是


请回答下列问题:
已知:Ksp(Ag2S)≈1.0×10-50 , Ag+ (aq)+ 2(aq)
[ Ag(S2O3)2]3- (aq),K稳≈1.0×1013(K稳表示配离子的稳定常数)。
①工业上,用电解法提纯银,装置如图。一段时间后,U形管中c(AgNO3)会(填“ 增大”“减小”或“不变”)。

②生活中银器、银首饰变暗的原因是银与空气接触时硫化氢和氧气参与反应,生成黑色Ag2S。恢复方法是:将变暗的银首饰等浸入盛装饱和食盐水的铝盆一段时间,银首饰“光亮如初”,其原理是: 2Al+3Ag2S+6H2O=2Al(OH)3 +6Ag+3H2S↑,正极的反应式为。
甲设计如下实验方案:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+ H2O
实验 | 0.1 mol·L-1 Na2 S2O3 (aq)/mL | 0.1 mol·L-1 H2SO4 (aq)/mL | 蒸馏水/mL | 温度/℃ | 出现浑浊 时间/s |
I | 10.0 | 10.0 | 0 | 25 | a |
II | 10.0 | 5.0 | V | 25 | b |
III | 10.0 | 10.0 | 0 | 35 | c |
实验结果:b>a>c。
V=。
乙设计实验测定硫代硫酸钠样品纯度:
步骤1:称取10.0g样品溶于水配制成250mL溶液。
步骤2:用碱式滴定管准确量取20. 00 mL配制溶液于仪器A中,滴几滴溶液B。
步骤3:用仪器C盛装标准0.1 mol·L-1 I2溶液并滴定步骤2中溶液至终点,做三次平行实验,测得消耗滴定液平均体积为25. 00 mL。已知:滴定反应为2 Na2S2O3+I2=2NaI+ Na2S4O6。
仪器A是(填名称,下同),溶液B是。仪器C是。

反应2的离子方程式为。上述转化中能量转化形式是太阳能→电能→能。
反应1:C(s)+ H2O(g) CO(g)+H2(g) ΔH1=+131.4 kJ·mol-1
反应2:CO(g)+ H2O(g) CO2(g)+H2(g) ΔH2=-41.1 kJ·mol-1
一定温度下,在恒容密闭容器中投入足量炭粉和1 mol H2O(g)发生上述反应,起始压强为0.2 MPa。测得H2O(g)的转化率与温度的关系如图所示。
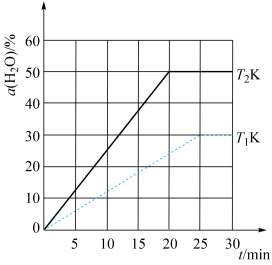
①C(s) +2H2O(g) CO2(g)+ 2H2(g) ΔH=kJ·mol-1。
②T1T2(填“>”“<”或“=”)。
③T2K下,达到平衡时CO为0.1mol,此时,反应体系中(填“吸收”或“放出”)热量为kJ。
④T2K下,反应1的平衡常数Kp=MPa。(提示:用分压计算的平衡常数为Kp , 分压=总压 ×物质的量分数)
⑤T2K下,0~20min内H2的分压变化率为 MPa· min- 1。

已知:H-N键的共用电子对偏离H,H-B键的共用电子对偏向H。H、B、N元素的电负性由大到小排序为(填元素符号)。

①起始时c( HSCN)c(CH3CO-COOH)(填“>”“<”或“=”),判断的依据是。
②c(OH-) :ab(填“>”“<”或“=”),判断的依据是。
③=3时,加热上述两种溶液,
会(填“增大”减小”或“不变”)(不考虑酸挥发等损失)。
④等体积、等物质的量浓度的KSCN溶液(X)、CH3COCOOK溶液(Y)中,离子总浓度:XY(填“>”“<”或“=”)。
①室温下,CH3COCOOH的电离常数Ka为。
②用平衡移动原理解释“缓冲原理”:。