 和
和  互为同分异构体
互为同分异构体



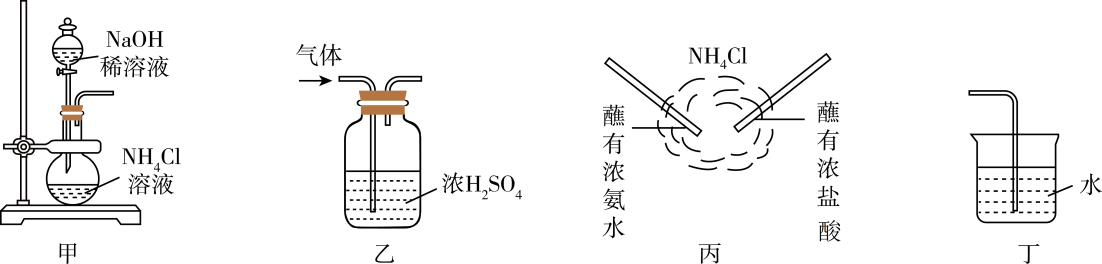
i.甲试管中反应的化学方程式是;反应类型是。
ii.浓硫酸的作用是:。
iii.分离出试管乙中油状液体的方法是,用到的主要仪器是。
a.与乙酸互为同系物
b.能发生加成、酯化、氧化反应
c.能与溶液反应生成
d.一定条件下能发生加聚反应,生成![]()
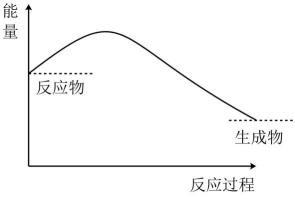
该反应为反应(填“吸热”或“放热”)。
实验编号 | 水果种类 | 电极间距离/cm | 电流 |
|
1 | 番茄 | 1 | 98.7 | |
2 | 番茄 | 2 | 72.5 | |
3 | 苹果 | 2 | 27.2 |
该实验目的是研究水果种类和对水果电池电流大小的影响。

由图中数据分析,该反应的化学方程式为。