选项 | 实验目的 | 实验方案设计 | 现象和结论 |
A | 证明碳酸钠遇水放热 | 向碳酸钠粉末中加少量水,观察现象并用手碰触试管外壁 | 结块,试管外壁变热,说明生成含有结晶水的碳酸钠晶体,同时放出热量 |
B | 蛋白质在某些物质作用下变性 | 向蛋白质溶液中加入浓 | 得白色浑浊,说明蛋白质发生了变性 |
C | 检验1-溴丁烷消去产物 | 取适量 | 酸性 |
D | 证明某无色溶液中含有 | 取少量溶液,加入盐酸后,滴入 | 滴入 |
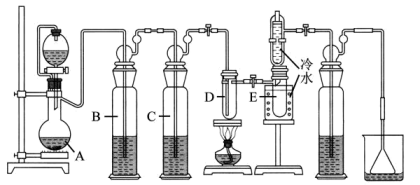
【相关药品性质】
药品 | 颜色、状态 | 熔点(℃) | 沸点(℃) | 其他性质 |
银白色固体 | 231 | 2260 | 较活泼金属能与 | |
无色液体 | 114 | 极易水解产生 |
请回答下列问题:
氯化物 | |||
沸点(℃) | 76 | 623(分解)* | 114 |
*注:加热至623℃,未沸腾直接分解
解释表中氯化物沸点差异的原因。

①两步反应的最佳温度为35℃,当温度低于5℃,反应接近停止的原因是;
②步骤I中若的消除速率为
, 则
的消耗速率为
;
①吹脱时,与
在溶液中存在下述平衡:
, 如图是不同温度下,水中
与
随
变化的相对含量图:

由图像可知,越大,水中
含量越高,其原因是。50℃平衡
的平衡常数
;
②氧化原理如下:

(i)其他条件相同时,向一定体积的氨氮废水中通入 , 根据上述原理推测下列说法错误的是(填代号);
a.该过程中N元素既有被氧化的过程又有被还原的过程
b.优良的催化剂不但能降低的活化温度,还能提升
的平衡转化率
c.单位时间内生成的活性氧(O·)越多,对转化为无害物越有利
d.随着温度升高、单位时间内的转化率提升说明该转化一定是吸热反应
(ii)其他条件相同,不同催化剂X、Y在发生催化作用时,对比结果如下:
催化剂 | 转化温度(℃) |
|
|
X | 250 | 90 | 50 |
Y | 225 | 90 | 90 |
X催化剂Y催化剂(填“优于”或“劣于”);
其原理为电解时阳极产生的羟基自由基氧化或
成为
而被去除。实验结果表明,当溶液中存在
时,
或
转化率大幅提升(如图所示),其可能的原因是。


请回答下列问题:

“操作1”需选择“高压浸出”的理由是;
a.其原理属于热还原法冶金
b. 的金属活动性可能位于
、
之间
c.工业上可用与钼酸盐溶液直接作用冶炼钼

请回答下列问题:
(i)![]()
(ii)![]()
试从绿色化学的角度评价两种方法的优劣;