 称量
B .
称量
B . 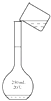 转移
D .
转移
D . 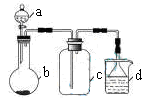
| 选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 浓硫酸(70%) | Na2SO3 | SO2 | NaOH溶液 |
| C | 稀硝酸 | Cu | NO2 | H2O |
| D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |

已知:焦亚硫酸钠是常见的抗氧化剂,在空气中、受热均易分解;
酸性:
请回答: