一、选择题(本题有15小题,每小题4分,共60分。请选出各题中一个符合题意选项)
-
A . 白玉做床,金做马
B . 千里冰封,万里雪飘
C . 野火烧不尽,春风吹又生
D . 夜来风雨声,花落知多少
-
A . 标签受损  B . 试管炸裂
B . 试管炸裂  C . 酒精溅出
C . 酒精溅出  D . 读数不正确
D . 读数不正确 
-
3.
不同洗手液pH一般不同,25℃时四种洗手液的pH如图所示。下列说法错误的是( )

A . 洗手液a用蒸馏水稀释后pH减小
B . 洗手液b的酸性比a弱
C . 洗手液c能使石蕊试液变蓝色
D . 洗手液d和a混合液的pH可能等于7
-
4.
稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,下列操作及实验现象(或结果),不能证明反应发生的是( )
A . 在混合液中加金属Zn,无气泡产生
B . 在混合液中加无色酚酞,溶液呈无色
C . 在混合液中加AgNO3溶液,有白色沉淀
D . 用pH试纸测混合液的pH,pH等于7
-
5.
若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是( )
A . Fe+MnSO4=FeSO4+Mn
B . Mg +MnSO4=MgSO4+Mn
C . Mn+Cu(NO3)2=Mn(NO3)2+Cu
D . Mn+2HCl=MnCl2+H2↑
-
6.
下列试剂中,能把KOH溶液、稀硫酸、CaCl2溶液一次鉴别出来的是( )
A . BaCO3
B . K2CO3
C . NaNO3
D . HCl
-
7.
下列各组物质中,同时放入pH=11的溶液中,能得到无色透明溶液的是( )
A . CuSO4、H2SO4、FeCl3
B . NaCl 、BaSO4、KOH
C . KOH、HCl、NaCl
D . HCl、HNO3、AgNO3
-
8.
实验室发现一瓶标签脱落的固体试剂,小王分别取少量的该固体进行了下列实验。根据实验现象,该固体最可能是( )
|
实验步骤
|
实验现象
|
|
检测水中加入固体前后液体的pH
|
固体不溶解,液体的pH几乎没变化
|
|
检测盐酸中加入固体前后溶液的pH
|
固体溶解,无气体放出,溶液pH增大
|
A . 金属单质
B . 非金属单质
C . 碳酸盐
D . 金属氧化物
-
9.
我国发明的新型钛合金,为“奋斗者”号下潜万米海底、从事科考任务解决了材料难题。工业制取金属钛的主要反应式是:
①2FeTiO3+6C+7Cl2  2FeCl3+2TiCl4+6CO ②2Mg+TiCl4
2FeCl3+2TiCl4+6CO ②2Mg+TiCl4  2MgCl2+Ti,
2MgCl2+Ti,
下列说法合理的是( )
A . FeTiO3属于氧化物
B . 钛合金是一种金属单质
C . 反应②属于置换反应
D . TiCl4中钛元素和氯元素的质量比为96∶71
-
10.
北宋沈括在《梦溪笔谈》中记载了用“苦泉水”制取铜的方法,其主要生产流程如图所示。下列解释合理的是( )
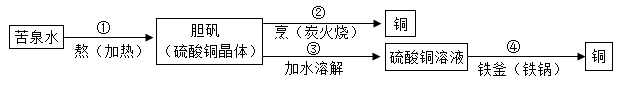
A . ①通过蒸发溶剂可获得晶体
B . ②是通过复分解反应获得铜
C . ③所得硫酸铜溶液一定是饱和的
D . ④说明铁元素变成了铜元素
-
11.
向盛有50mL稀硫酸的烧杯中,缓慢滴加一定溶质质量分数的氢氧化钡溶液至过量。随着氢氧化钡溶液的滴加,某些量变化趋势正确的是( )
-
12.
下列除杂质的方法错误的是( )
| | 物质(括号内为杂质) | 除杂方法 |
| A | NaCl(泥沙) | 溶解、过滤、蒸发 |
| B | FeCl2溶液(CuCl2溶液) | 加入过量铁粉、过滤 |
| C | CaCl2溶液(盐酸) | 加入过量CaCO3、过滤 |
| D | CO2(CO) | 通入澄清石灰水 |
A . A
B . B
C . C
D . D
-
A . 氯化钾
B . 过磷酸钙
C . 硫酸钾
D . 尿素
-
14.
如图所示,装置气密性良好,弹簧夹处于关闭状态.挤压胶头滴管加入液体,一段时间后,打开弹簧夹,能使气球a明显鼓起的是( )

| |
试管内物质
|
胶头滴管内物质
|
|
A
|
氢氧化钠固体
|
水
|
|
B
|
铁
|
稀盐酸
|
|
C
|
氯化钡溶液
|
稀硫酸
|
|
D
|
二氧化碳
|
氢氧化钠溶液
|
A . A
B . B
C . C
D . D
-
15.
向一定质量的Mg(NO
3)
2和Cu(NO
3)
2混合溶液中加入
a克锌粉和铁粉的混合物,充分反应后过滤,得到不饱和的滤液和滤渣,将滤渣洗涤、干燥后再称量,得到的固体质量仍为
a克。下列分析合理的是( )
①滤渣中可能有铜
②向滤渣中加稀盐酸,可能有气泡产生
③滤液中一定有Mg(NO3)2、Zn(NO3)2和Fe(NO3)2 , 可能有Cu(NO3)2
④若忽略过滤操作中溶液损失,滤液中溶质的质量一定大于原混合溶液溶质的质量
A . ①②
B . ①③
C . ②③
D . ②④
二、简答题(本题有9小题20空,每空2分,共40分。)
-
16.
小明在用碱水洗桃毛时发现了一个奇怪的现象,桃表面的颜色从粉红色变成紫黑色。他想这是正常现象还是商贩用化学药水泡过呢?
查阅资料发现:桃子的红色来源于天然色素—花青素,它在酸性条件下呈红色,碱性下会变蓝色,如颜色比较深就呈现紫黑色,中性呈紫色。
-
(1)
洗桃子用的碱水可能是 的水溶液(填化学式)。
-
(2)
利用花青素可以辨别的物质是
A . 盐酸和硫酸
B . 硫酸和氯化钠溶液
C . 氢氧化钾溶液和盐酸
D . 氢氧化钠溶液和氢氧化钾溶液
-
17.
在实验室做酸和碱与指示剂反应的实验,所用试剂如图所示,实验后把废液集中倒入废液缸中。

-
-
-
18.
最近报道,慢性腹泻患者宜喝酸牛奶,酸牛奶中酪蛋白易于消化吸收,能使胃容物的酸性增强,还可促进钙的吸收。
-
(1)
喝酸牛奶后,胃容物的pH(填“增大”或“减小”)。
-
(2)
“钙尔奇D”是一种常见的补钙剂,如图是“钙尔奇D”说明书的一部分。根据以上信息:写出胃液与“钙尔奇D”反应的化学方程式
。

-
19.
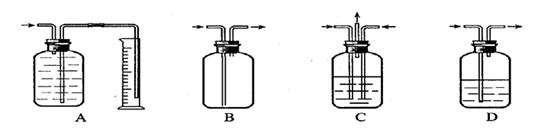
广口瓶被称为气体实验的“万能瓶”,它可以配合玻璃管和其他简单仪器组成各种功能的装置。
-
(1)
A装置是用来收集气体并测量瓶内收集气体的体积,这种收集气体体积的方法。
-
(2)
C装置可以作为某些反应的发生器,在该装置中按图中箭头的要求进行的反应是 。
A . NH3 +H2O+CO2=NH4HCO3
B . 2NH3 + H2SO4 =(NH4)2SO4
C . CaCO3+H2O+CO2=Ca(HCO3)2
D . CH4+2O2  2H2O+CO2
2H2O+CO2
-
(3)
D装置可以用来干燥某些气体,若要干燥氢气,则在广口瓶内装的液体是
。
该装置也可以用来洗气,若瓶内装的是硝酸银溶液,则可以洗去的气体是。
-
20.
图中的A、B、C、D、E为常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系。请回答:

-
-
(2)
步骤②中发生的反应属于酸中的哪一条通性:。
-
(3)
写出步骤③中所发生反应的其中一个化学方程式。
-
21.
二氧化碳的资源化利用是实现碳减排的重要途径。以下是一种实现二氧化碳转化为重要原料二甲醚(化学式为C
2H
6O)的途径:

-
(1)
转化①是二氧化碳与一种常见单质反应生成甲醇和水,这种单质的化学式。
-
(2)
转化②是甲醇发生分解反应生成二甲醚和水,反应中生成二甲醚和水分子数的比为。
-
22.
从HCl、NaCl、NaOH、Na
2CO
3、Ca(OH)
2几种溶液中取出其中的两种混合进行相关实验。

-
(1)
若两种溶液混合后溶液的总质量减小,则它们的组合可能是:。
-
(2)
将稀硫酸逐滴滴入某种组合后的溶液中,若产生气体与加入稀硫酸如图所示的关系,则这样的组合可能是。
-
23.
扑克是生活中用来休闲的娱乐项目之一,聪明的小华发明了一种扑克新玩法-“化学扑克”。“化学扑克”的玩法是:上家出牌,如果下家牌中的物质能与上家的发生反应,即可出牌,按此规则,出完牌的为赢家。下图表示的是某局牌的最后一轮。桌面上是一张图甲的“盐酸”牌,ABCD四位玩家手中都剩下一张牌(如图)。

-
(1)
如果本局每一位玩家的牌都能出掉,则四位玩家的出牌顺序为:(填标号)甲→;
-
(2)
如果本局只有一位玩家的牌出不掉,他们的出牌顺序为:(填标号)甲→。
-
24.
(2019九上·温州月考)
小科到野外郊游,不小心被蚊虫叮咬,蚊虫能分泌蚁酸,蚁酸酸性很强,有腐蚀性,能刺激皮肤起泡,引起肿痛。下列物质可用手涂抹以减轻疼痛的有
(填字母)。
A . 纯碱溶液
B . 石灰水
C . 肥皂水
D . 氢氧化钠溶液
三、实验探究题(本题有7小题20空,每空3分,共60分。)
-
25.
丙烷(C
3H
8)作为一种燃料,其燃烧后的产物是什么?某环保小组的同学在老师的指导下选择了如下装置(铁架台等装置已略去),对丙烷在氧气中燃烧后的气体进行了检测(补充:CuO+CO

Cu+CO
2)

-
(1)
根据所选的装置分析,该小组同学猜测丙烷燃烧后的气体可能含有。
-
(2)
将上述装置按一定顺序连接完整,使之尽可能检测出丙烷燃烧后的产物。你设计的连接顺序为:燃烧后的气体 →B→D。
-
(3)
该小组的同学按合理的连接顺序进行检测.实验过程中观察到的部分现象如下:A装置中的澄清石灰水变浑浊,C装置中的无水硫酸铜变蓝,D装置中的澄清石灰水无明显现象。根据以上现象分析可知,丙烷在氧气中燃烧后的气体为。
-
-
26.
实验室常用锌和稀硫酸来制取氢气,向盛有稀硫酸溶液的烧杯中加入足量的锌至反应完全。

-
-
(2)
如图的“

”“〇”“●”表示溶液中由溶质电离产生的不同离子,则“●”表示
。(离子符号)
-
27.
(2019九上·温州月考)
某氯化钠固体样品中含有少量的 MgCl
2、CaCl
2 和 Na
2SO
4 , 为除去其中的杂质,某同学设计了以下实验方案:先将固体充分溶解,然后依次向其中加入过量 BaCl
2 溶液、过量NaOH 溶液、过量Na
2CO
3 溶液和适量稀盐酸,充分反应后过滤,然后再蒸发结晶。
请回答:
-
(1)
溶解、过滤和蒸发操作中都用到一种玻璃仪器,该仪器在过滤操作中的作用是。
-
(2)
预测加入过量NaOH 溶液时观察到的现象是。
-
(3)
上述实验方案是否合理?若不合理,如何改正?。
-
28.
某实验小组为了探究影响化学反应速率的因素,进行了稀硫酸与金属铁反应的对照实验,实验数据如下:
|
实验序号
|
金属质量/g
|
金属状态
|
H2SO4
质量分数%
|
V(H2SO4)
/mL
|
反应前溶液温度/℃
|
金属消失的时间/s
|
|
1
|
0.10
|
丝
|
5
|
50
|
20
|
500
|
|
2
|
0.10
|
粉末
|
5
|
50
|
20
|
50
|
|
3
|
0.10
|
丝
|
10
|
50
|
20
|
125
|
|
4
|
0.10
|
丝
|
10
|
50
|
35
|
50
|
-
(1)
根据以上实验数据分析可得,影响化学反应速率的因素有。
-
-
29.
某溶液中,只可能含有以下离子中的若干种:K
+、NH
4+、Cl
-、Mg
2+、Ba
2+、CO
32-、SO
42- , 现取三份各100mL溶液进行如下实验:
第一份加入AgNO3溶液有沉淀产生。
第二份加足量NaOH溶液加热,有气泡冒出并闻到刺激性气味。
第三份加足量BaCl2溶液后,得到干燥沉淀12.54 g,经足量盐酸洗涤、干燥后,沉淀质量为4.66 g。
根据上述实验,回答以下问题:
-
(1)
由第一份进行的实验推断该溶液中是否一定含有Cl-并说明理由。
-
-
(3)
由第三份进行的实验可知12.54g沉淀的成分为。
-
30.
某化学兴趣小组向一定量的AgNO
3和Cu(NO
3)
2混合溶液中加入一定量的Mg粉,充分反应后过滤得溶液A和固体B。对滤液A所含的溶质有以下几种猜想:
①Mg(NO3)2、AgNO3、Cu(NO3)2 ②Mg(NO3)2、Cu(NO3)2
③Mg(NO3)2、AgNO3 ④只有Mg(NO3)2
-
(1)
经过讨论,大家一致认为不合理的猜想是(填标号)。
-
(2)
若猜想④成立,通过以下实验可确定固体B的成分,请将下表填写完整。
-
31.
某兴趣小组同学发现实验台上整齐摆放的药品中(如图),有一试剂瓶的标签受损。




【提出问题】这瓶试剂是什么?
【讨论、猜想】可能是Na2SO4溶液;也可能是NaOH溶液;还可能是……。
【设计与实验】
-
(1)
甲同学根据受损标签及实验室药品分类摆放的原则,认为如果是NaOH溶液可以不用做实验只要看一下就可以分辨,你认为甲同学能这么快分辨的理由是。
-
(2)
乙同学用上图已有的试剂做实验,鉴别出了该试剂就是Na
2SO
4溶液。
四、分析计算题(本题有5小题,第32题6分,第33题6分,第34题10分,第35题10分,第36题8分共40分)
-
32.
小明在化学晚会上观看了“瓶吞鸡蛋”的魔术(如图1),看到鸡蛋被吞进瓶内。小明思考:瓶能吞蛋,能不能吐蛋呢?他进行了如图2的实验,他加入的试剂 p,结果鸡蛋吐了出来。请判断小明所加试剂p的名称,并利用所学知识,解释鸡蛋被吞进瓶内和吐出来的原因。

-
33.
某学校在进行植物园建设时设置了一个无土栽培区。无土栽培是利用磷酸钙、碳酸钾和氯化铵等盐类配置营养液栽培植物的一种方法。很多学生对此很感兴趣,并进行了研究和实践。
-
(1)
无土栽培时,营养液浓度不宜过高,其原因是。
-
(2)
氯化铵(NH4Cl)中氮元素和氢元素的质量比为。
-
(3)
小明在某次配制营养液时需要加入
14 克氮元素,如果这些氮元素都由氯化铵提供,则需要加入多少克氯化铵?(写出计算步骤)
-
34.
实验室用足量的稀盐酸和大理石制取CO
2 , 为了分析反应后滤液的成分,取100g反应后的滤液,逐滴滴入溶质质量分数为20.0%的Na
2CO
3溶液,测得滴加溶液的质量与产生沉淀的关系如图。回答下列问题:(已知:CaCl
2溶液呈中性)

-
(1)
从开始加入碳酸钠溶液至10g时,没有产生沉淀的原因是。
-
-
-
35.
为了测定某黄铜(铜和锌的合金)样品中铜的质量分数,取10克该黄铜样品加入100克稀硫酸中,恰好完全反应,产生氢气0.2克。
-
(1)
实验室里的稀硫酸是用浓硫酸稀释而成,在配制稀硫酸时,应该先向烧杯中倒入定量的(选“浓硫酸”或“水”)。
-
(2)
需用多少克质量分数为98%的浓硫酸来稀释?
-
-
36.
某碱的化学式是M(OH)
x(M代表金属元素),它的相对分子质量是171。用3.65%的盐酸和17.1%的M(OH)
x溶液在下图所示的井穴板中进行反应,每一井穴中都加入石蕊试液作指示剂。

加入试剂的量(假设不同试剂每滴的质量都相同)及颜色变化如下:
|
井穴编号(从左到右)
|
①
|
②
|
③
|
④
|
⑤
|
⑥
|
|
盐酸/滴
|
0
|
2
|
4
|
8
|
10
|
12
|
|
M(OH)x溶液/滴
|
12
|
10
|
8
|
4
|
2
|
0
|
|
颜色变化
|
蓝
|
蓝
|
蓝
|
紫
|
红
|
红
|
-
(1)
在6个井穴中,HCl和M(OH)x恰好反应完全的是(填编号),理由是。
-
 B . 试管炸裂
B . 试管炸裂  C . 酒精溅出
C . 酒精溅出  D . 读数不正确
D . 读数不正确 

