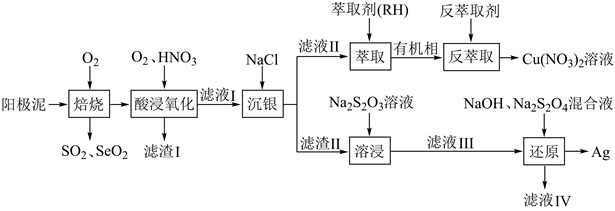
已知:①该工艺中萃取与反萃取原理为: ;
② 易与 Ag+形成配离子:
,常温下该反应的平衡常数
。
回答下列问题:
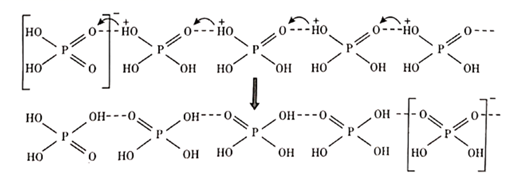
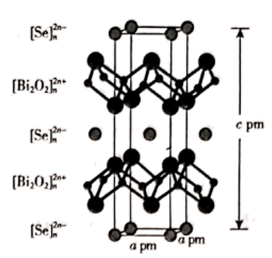
由此可以推知纯磷酸液体中存在的导电微粒是 和,
的空间构型为。
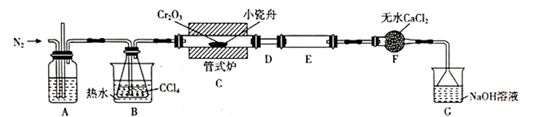
已知:①COCl2(俗称光气)有毒,遇水发生水解: ;
②碱性条件下,H2O2将Cr3+氧化为 ;酸性条件下,H2O2将
还原为Cr3+。
回答下列问题:
I.取m g CrCl3产品,在强碱性条件下,加入过量的30% H2O2溶液,小火加热使 CrCl3完全转化为 ,继续加热一段时间;
Ⅱ.冷却后加适量的蒸馏水,再滴入适量的浓硫酸和浓磷酸(加浓磷酸的目的是为了防止指示剂提前变色),使 转化为
;
Ⅲ.用新配制的 标准溶液滴定至终点,消耗
标准溶液V mL(已知
被 Fe2+ 还原为Cr3+)。
①产品中 CrCl3 质量分数表达式为。
②下列操作将导致产品中 CrCl3质量分数测定值偏低的是(填标号)。
a.步骤Ⅰ中未继续加热一段时间
b.步骤Ⅱ中未加浓磷酸
c.步骤Ⅲ中所用 溶液已变质
d.步骤Ⅲ中读数时,滴定前俯视,滴定后平视
I.
Ⅱ.
回答下列问题:
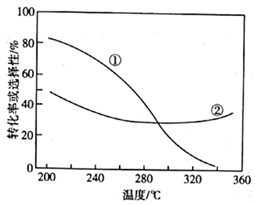
已知: 的选择性=
×100%。其中表示平衡时
的选择性的是曲线(填"①"或"②");温度高于 300℃时,曲线②随温度升高而升高的原因是;为同时提高 CO2的平衡转化率和平衡时
的选择性,应选择的反应条件为(填标号)。
a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
①为提高 CH3OCH3的平衡产率,可以采取的措施有(任写一条)。
②473 K时,在密闭容器中加入一定量 CH3OH(g),采用合适的催化剂进行反应,达到平衡时体系中 CH3OCH3(g)的物质的量分数为(填标号)。
a.< b.
c.
~
d. >
①降低温度,k正-k逆(填"增大"、"减小"或"不变");
②在TK、101kPa下,按照 投料,CO2转化率为50%时,
,用气体分压表示的平衡常数 Kp=。