 分离碘和酒精
B .
分离碘和酒精
B . 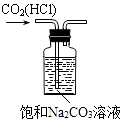 除去CO2中的HCl
C .
除去CO2中的HCl
C . 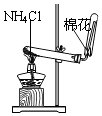 实验室制氨气
D .
实验室制氨气
D . 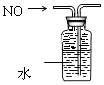 排水法收集NO
排水法收集NO
元素编号 | 元素性质与原子(或分子)结构 |
W | 周期表中原子半径最小的元素 |
X | 氢化物可与其最高价氧化物的水化物反应生成盐 |
Y | 一种核素在考古时常用来鉴定一些文物的年代 |
Z | M层比K层少1个电子 |
T | 存在两种同素异形体,其中一种可吸收紫外线 |
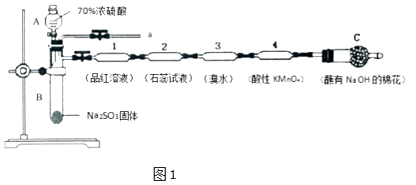
回答下列问题:

①装置A中试剂X是;装置1中反应的化学方程式是.
②实验结论:因为酸性强弱是>>(填化学式),故非金属性是S>C>Si.