选择题
试题详情
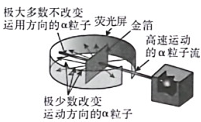
1909年起,英国科学家卢瑟福和他的助手用一束带正电荷的高速α粒子流轰击一片很薄的金箔,并根据如图所示的实验现象和已有知识,在1911年提出了原子的有核模型。要解释本实验现象产生的原因,下列知识不需要用到的是………………( )
- A、 同种电荷相互排斥
- B、 电荷的定向移动形成电流
- C、 力是改变物体运动状态的原因
- D、 一个α粒子的质量比一个电子的质量大得多
试题详情
替诺福韦(化学式为C₉H₁₄N₅O₁P)是一种抗病毒药物,在55℃~65℃的环境中反应制成,其相对分子质量为287.22。下列关于它的表述正确的一项是………………………………………( )
- A、 受热即可分解
- B、 属于混合物
- C、 质量为287.22
- D、 由五种元素组成
试题详情
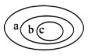
分类法是科学学习常用的一种方法,下列选项符合如图所示关系的是……………………………………( )
选项 | a | b | C |
A | 原子 | 原子核 | 质子 |
B | 单质 | 化合物 | 臭氧 |
C | 金属 | 非金属 | 汞 |
D | 纯净物 | 混合物 | 冰水混合物 |
- A、 A
- B、 B
- C、 C
- D、 D
试题详情
下列说法正确的是…………………………………………( )
- A、 原子核内的质子数和核电荷数一定相等
- B、 原子核中的质子数和中子数一定相等
- C、 原子核一定是由质子和中子构成的
- D、 元素的化学性质取决于原子核内的质子数
试题详情
化学上常用左下角的数字表示原子的质子数,左上角的数字表示原子的中子数与质子数之和,如 表示核内有6个质子和7个中子的碳原子。下列关于
表示核内有6个质子和7个中子的碳原子。下列关于 和
和 的说法中错误的是 ( )
的说法中错误的是 ( )
- A、 两种原子相比较,质子数相同
- B、 两种原子相比较,中子数相同
- C、 两种原子相比较,核外电子数相同
- D、 属于同种元素
试题详情
2017年,哈佛大学科学家利用约488万个大气压制成了世界首个金属氢,如图所示。下列有关叙述正确的是( )
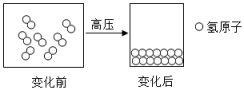
- A、 氢气是由两个氢元素组成的
- B、 氢气和金属氢是由氢原子构成的
- C、 金属氢中氢元素的化合价是0
- D、 金属氢中的原子含有质子、中子和电子各1个
填空题
试题详情
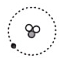
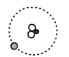
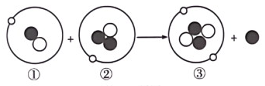
如图为核聚变的示意图,其中①②③表示三种原子,“●”“O”“o”表示原子中的不同粒子,“●”表示,①②③中互为同位素原子的是(填序号),核聚变(填“是”或“不是”)化学变化。
试题详情
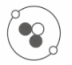
探测月壤是“嫦娥一号”的主要任务之一。因为月壤中蕴藏着丰富的He-3,其原子结构如图所示。He-3是一种安全、高效的清洁燃料,它的应用前景十分广阔。请回答下列问题。
试题详情
铝原子(Al)和铝离子(Al³⁺)属于同一种元素,因为它们的相同。Al和Al+属于(填“相同”或“不同”,下同)的粒子,因为它们的核外电子总数。
试题详情
如图代表氢的三种原子的原子核。请回答下列问题。

试题详情
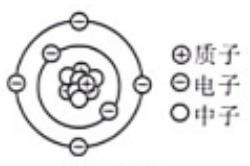
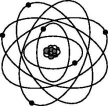
建立模型一般有一个不断完善和修正的过程,以使模型不断接近事物本质,原子结构模型的建立也是如此,其中行星模型的建立是一个重要阶段。如图是碳原子结构的行星模型,表示碳原子核内有6个和6个中子;核外有6个,且围绕原子核做高速运动;原子核在原子中所占的体积。
试题详情
通过分析下表,你能得出哪些结论?
| 原子种类 | 核电荷数 | 质子数 | 中子数 | 核外电子数 |
| 氢原子 | 1 | 1 | 0 | 1 |
| 碳原子 | 6 | 6 | 6 | 6 |
| 原子种类 | 核电荷数 | 质子数 | 中子数 | 核外电子数 |
| 氧原子 | 8 | 8 | 8 | 8 |
| 钠原子 | 11 | 11 | 12 | 11 |
结论1:。
结论2:。
结论3:。
结论4:。
实验探究题
试题详情
人们为了解释原子结构的奥秘,经历了漫长的探究过程。1803年,道尔顿提出原子概念,他认为一切物质都是由原子构成的。1897年,汤姆生发现原子中存在一种带负电荷的粒子,证明原子是可以再分的,又提出了“面包模型”。1911年,英国科学家卢瑟福为探索原子的内部结构,用带正电的α粒子轰击金属箔,发现如下现象:①大多数α粒子能穿透金属箔而不改变原来的运动方向;②有小部分α粒子改变了原来的运动方向;③有极少部分α粒子被弹了回来。请回答:
试题详情
卢瑟福用α粒子(α粒子是带两个单位正电荷的氦原子核)轰击金箔的实验,推翻了汤姆在 1903 年提出的原子结构模型,为建立现代原子理论打下了基础(如图)。
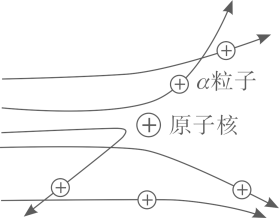
现象 1:大多数α粒子能穿透金箔而不改变原来的运动方向。
现象 2:一小部分α粒子改变原来的运动方向。
现象 3:极少数α粒子被弹了回来。
试题详情
探究原子结构的奥秘:1803年英国科学家道尔顿提出了近代原子学说,他认为一切物质是由原子构成的,这些原子是微小的不可分割的实心球。1911年,英国科学家卢瑟福用一束平行高速运动的α粒子(α粒子是带两个单位正电荷的氦原子)轰击金箔时(金原子的核电荷数为79,相对原子质量为197),发现大多数α粒子能穿透金箔,而且不改变原来的运动方向,但是也有一小部分α粒子改变了原来的运动路径,甚至有极少数的α粒子好像碰到了坚硬不可穿透的质点而被弹了回来。
解答题
试题详情
征服原子——揭开原子的神秘面纱。请回答下列问题。