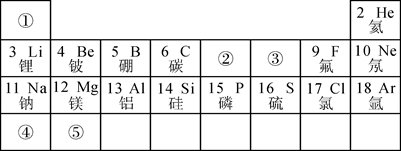
选择题
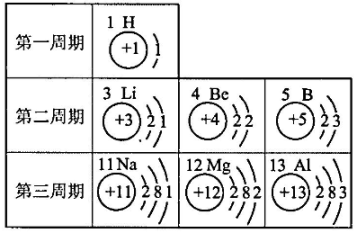
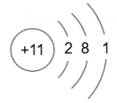
- A、 同一周期元素的最外层电子数相同
- B、 钠离子核外有三个电子层
- C、 第二、三周期元素的原子从左到右最外层电子数逐渐增多
- D、 在化学变化中镁元素容易失去最外层的2个电子形成镁离子,其离子符号是Mg⁺₂
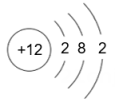
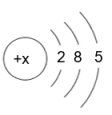
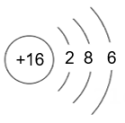
- A、 该元素位于元素周期表第二周期
- B、 该粒子为阴离子
- C、 该粒子核电荷数为 10
- D、 该粒子带正电
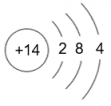
- A、 H 只表示氢元素
- B、 Fe 表示铁元素,表示一个铁原子,表示铁这种物质
- C、 N 只表示一个氮原子
- D、 0 表示氧元素,表示一个氧原子,表示氧气这种物质
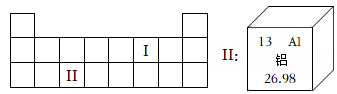
全球近140个国家将根据签署的《国际防治汞污染公约》,在2020年前禁止生产和出口含汞产品,如电池、荧光灯、化妆品、温度计、血压计等,分析如图判断关于汞元素的相关信息正确的是( )

- A、 汞的化学式为Hg
- B、 汞原子的质量为200.6g
- C、 汞原子的中子数是80
- D、 汞为非金属元素
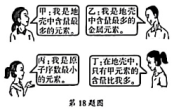
- A、 地壳中元素含量由高到低
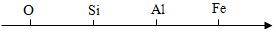
- B、 不同种原子的原子序数依次递增
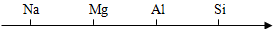
- C、 空气中气体体积分数由大到小

- D、 含氮物质中氮元素的化合价从低到高

- A、 Cl既可以表示氯元素,也可以表示一个氯原子
- B、 在化学变化中,分子可以再分,原子不能再分
- C、 石墨和金刚石都是由碳元素组成的,所以石墨和金刚石混在一起的物质是纯净物
- D、 NO2中的“2”表示一个二氧化氮分子中有两个氧原子
| H | He | ||||||
| ① | N | ② | Ne | ||||
| ③ | Ar | ||||||
- A、 ①和②处于同一族
- B、 表中不同种元素最本质的区别是中子数不同
- C、 表中②所代表元素是金属元素
- D、 元素符号是N的原子核外电子数是7个
- A、 H2S、H2O、H2三种物质中都含有氢分子
- B、 H2SO3和H2SO4中硫元素的化合价相同
- C、 Na+、Mg2+、Al3+原子核内质子数均为10
- D、 由Na和K在元素周期表中的位置得出,钠元素和钾元素的化学性质相似
①N ②Fe ③Fe2+ ④H2O ⑤NaCl
- A、 ③表示铁离子
- B、 能表示一个分子的有①②④⑤
- C、 ②和③属于同种元素
- D、 ④表示H2O由2个氢元素和1个氧元素组成
填空题
5个钾原子:;2个氮气分子:;
3个氯离子:;硫酸亚铁:。
①黄金搭档,花一样钱补五样;
②葡萄糖酸锌口服溶液,蓝瓶的,好喝的。
请填写下列空白:
黄金搭档所补五样是指:钙(元素符号为)、铁、锌、硒、维生素。其中前四样是指人体需要这四样(填“单质”“离子”或“元素”)。
1829年,德国化学家德贝纳提出了锂钠钾、钙锶钡、磷砷锑、氯溴碘等15种元素,他把这些元素称为“三元素组”。
1864年,德国化学家迈耶,按相对原子质量递增顺序制定了一个“六元素表”。
1865年,英国化学家纽兰兹按相对原子质量递增顺序,将已知元素作了排列。发现第八个元素就与第一个元素性质相似(元素的排列每逢八就出现周期性)。这好像音乐上的八个音阶一样重复出现,于是提出“八音律”的理论(下表是“八音律表”的前部分)。
| H | Li | G | Bo | C | N | O |
| F | Na | Mg | Al | Si | P | S |
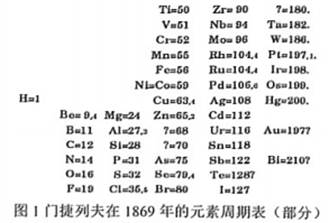
1869年,俄罗斯化学家门捷列夫对当时已知的63种元素的相对原子质量和物理性质(熔点、密度等)进行了比较,直到19世纪末才制成了第一张元素周期表。事实上,在1869年,德国的迈耶和俄国的门捷列夫几乎同时发现了元素周期律。分析上述科学史料,并结合当代的元素周期表的相关知识回答:
实验探究题
材料一:门捷列夫将元素按照相对原子质量从小到大排列后,发现元素的化学性质成周期性出现,故将相似化学性质的元素排在同一列。
材料二:门捷列夫无可非议地成为元素周期律的主要发现者,因为门捷列夫的元素周期表有强大的预测功能。
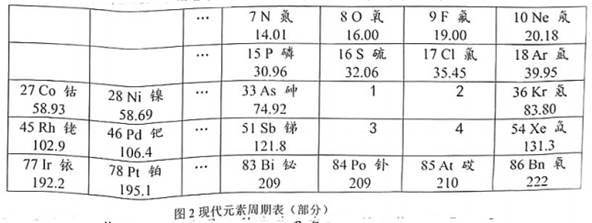
材料三:氟是一种非金属化学元素,氟元素的单质是F2 , 它是一种淡黄色有剧毒的气体。氟气的腐蚀性很强,化学性质极为活泼,是氧化性最强的物质之一。
硫是一种非金属元素,通常单质硫是黄色的品体。硫元素在自然界中通常以化合物或单质的形式存在。硫单质难溶于水,微溶于酒精对人体而言,单质硫通常是无毒无害的。