NO2 | CO | CO2 | NO |
812kJ | 1076kJ | 1490kJ | 632kJ |
②N2(g)+O2(g) 2NO(g) △H=+179.5kJ/mol K2
③2NO(g)+O2(g) 2NO2(g) △H=-112.3kJ/mol K3
写出NO与CO反应生成无污染气体的热化学方程式,该热化学方程式的平衡常数K=(用K1、K2、K3表示)。
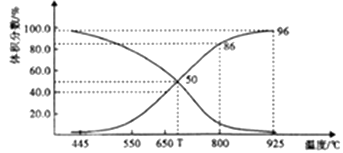
①T℃时,在容器中若充入稀有气体,v(正)v(逆)(填“>”“<”或“="),平衡移动(填“正向”“逆向”或“不”。下同);若充入等体积的CO2 和CO,平衡移动。
②CO体积分数为40%时,CO2 的转化率为。
③已知:气体分压(p分)=气体总压×体积分数。用平衡分压代替平衡浓度表示平衡Kp常数的表达式为;925℃时,Kp=(用含p总的代数式表示)。
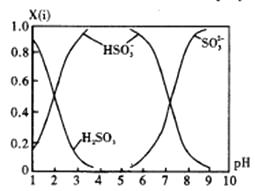
①若是0.1mol/LNaOH 反应后的溶液,测得溶液的pH=8时,溶液中各离子浓度由大到小的顺序是。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2 溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因。