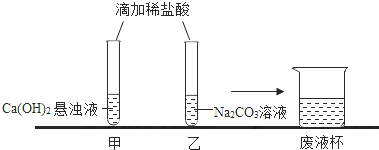
【观察与讨论1】甲同学在做实验时观察到的明显现象是.再滴加无色酚酞溶液,无明显现象(已知CaCl2溶液呈中性).
【观察与讨论2】乙同学在做实验时开始没有观察到气泡产生,于是对碳酸钠能否与盐酸反应表示怀疑.甲同学通过查阅资料得知:在碳酸钠溶液中滴加少量稀盐酸,先发生反应Na2CO3+HCl=NaCl+NaHCO3 , 继续滴加稀盐酸,再发生反应,NaHCO3+HCl=NaCl+H2O+CO2↑.所以甲同学认为,乙同学实验时还应继续滴加稀盐酸,才能观察到有气泡产生(已知NaHCO3溶液呈碱性).
【观察与讨论3】甲同学先将废液缓慢倒入一洁净的废液杯中,乙同学在观察到气泡产生后,也将实验废液缓慢倒入该废液杯中,没有观察到明显现象.为了处理实验后产生的废液,甲、乙同学决定对废液杯中最终废液溶质的成分进行探究.
【提出问题】最终废液中含有什么溶质?
【猜想与假设】猜想1:废液中含有NaHCO3、CaCl2、NaCl三种溶质.
猜想2:废液中含有(写化学式)三种溶质.
猜想3:废液中含有…溶质.
【实验与结论】甲、乙同学为了验证猜想,进行了如下实验:
甲同学实验:取少量废液于试管中,向其中滴加盐酸,有气泡产生.
乙同学实验:取少量废液于试管中,向其中滴加紫色石蕊试液,溶液变蓝色.
猜想(填“1”或“2”或“3”)正确.
【交流与反思】在分析化学反应后所得物质时,除考虑生成物外,还需要考虑