
|
|
|
|
怡宝饮用纯净水 | 铁强化酱油 | 金刚石的结构 | 干冰 |
①怡宝纯净水属于(填“纯净物”或“混合物”).
②铁强化酱油中的“铁”指的是(填“元素”、“原子”、或“分子”).
③金刚石是由构成的. ④干冰可用于(填一例).
①瓦斯的主要成分;②极易与血红蛋白结合的有毒气体;
③两个铵根离子;④过氧化氢中氧元素的化合价;
①煤、石油和天然气等化石燃料是能源(选填“可再生”或“不可再生”).将煤块粉碎成煤粉后燃烧,其目的是;煤燃烧时排放出,这些气体或气体在空气中发生反应后的生成物溶于雨水会形成酸雨.
②我国水资源丰富,但分布不均.有些村民用地下水作为生活用水,常向水中加入检验是硬水还是软水.生活中硬水软化的方法为.
③下列自来水的净化过程中发生化学变化的是.
A.自然沉淀 B.沙层过滤 C.活性炭吸附 D.杀菌消毒.

已知:白磷的着火点为40℃,红磷的着火点为240℃.
实验用品 | 实验现象 |
蘸有酒精的玻璃棒 | 产生火焰 |
蘸有水的玻璃棒 | 无明显变化 |
此现象能够说明燃烧应具备的条件是,实验中发生反应的化学方程式为.
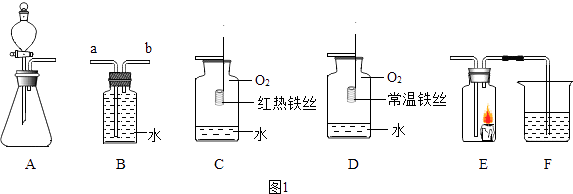
若用装置B排水收集氧气,气体从(填“a”或“b”)导管通入瓶内;瓶底留少量水进行装置C中的实验,水的作用是.
①若实验时E中蜡烛熄灭,F中溶液变浑浊,则A中反应的化学方程式为;E中蜡烛熄灭,说明A中产生的气体所具有的性质为.
②若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,则A中反应的化学方程式为.
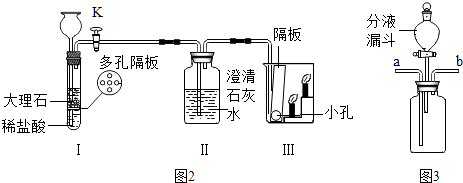
甲同学利用如图2装置对二氧化碳的性质进行验证.
关闭K,装置Ⅰ中能观察到的现象是;
作为制取二氧化碳的发生装置,装置Ⅰ的优点是.
①从b端通氮气 ②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中
③从a端通二氧化碳 ④从分液漏斗中滴加适量水.


据此小明得出蜡烛是由碳、氢元素组成的.你认为他的结论是否正确?.
实验步骤如下:
先分别称量蜡烛、装置Ⅱ(吸收水)、装置Ⅲ(吸收二氧化碳)的质量.
按图示连接好仪器,点燃蜡烛,同时从a导管口抽气.
一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量.
实验数据如表.请回答:
蜡烛 | 装置Ⅱ | 装置Ⅲ | |
反应前的质量/g | 15.8 | 182.3 | 212.2 |
反应后的质量/g | 14.4 | 184.1 | 216.6 |
①该实验中测得水的质量为 g.
②由该实验数据计算,蜡烛中碳、氢元素的质量之比为.
③理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是.
④该实验能否准确测出蜡烛燃烧生成二氧化碳和水的质量?说明理由..