一、选择题(本大题共15小题,每小题3分,共45分。每小题只有1个选项符合题意。请将符合题意的选项用 2B 铅笔填涂在答题卡相应位置
-
1.
我国古代文献记载中蕴含着丰富的化学知识。下列记载中不涉及化学变化的是( )
A . 《易经》——“泽中有火,上火下泽”
B . 《天工开物》:“凡石灰,经火焚炼为用”
C . 《抱朴子》——“丹砂(HgS)烧之成水银,积变又还成丹砂”
D . 《天工开物》——“侯潮一过,明日天睛,半日晒出盐霜”
-
-
3.
中国丝绸有几千年的历史传承。古代染坊常用某种“碱剂”来处理丝绸,该“碱剂”可使丝绸颜色洁白、质感柔软,该“碱剂”常从草木灰中提取,其主要成分是一种盐,这种“碱剂”可能是( )
A . 食醋
B . 火碱
C . 生石灰
D . K2CO3
-
4.
关于物质性质和用途的说法不对应的是( )
A . 碳酸氢钠能与盐酸反应,可治疗胃酸过多
B . 氢氧化钠易潮解,可作干燥剂
C . 活性炭有吸附性,可用于冰箱除异味
D . 氯化钠有咸味,可用于生产烧碱
-
5.
化学与生活是密切相关的,下列生活中的一些做法不可行的是( )
A . 用过滤的方法降低水的硬度;用泡沫灭火器去灭电线或电器着火
B . 用布袋代替塑料袋以防止白色污染;扫地前洒水以防止空气中的灰尘含量增加
C . 用蔗糖作为甜味剂添加到食品中;用搅拌的方法加速蔗糖溶解
D . 用洗洁精去除餐具上的油污;用白醋去除厨具上的铁锈
-
6.
如图是某元素在元素周期表中的相关信息,下列关于该元素说法错误的是( )
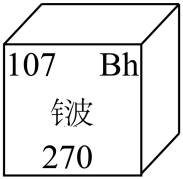
A . 元素符号为 B . 原子核外电子数为107
C . 属于金属元素
D . 该原子的质量为270
B . 原子核外电子数为107
C . 属于金属元素
D . 该原子的质量为270
-
7.
黑火药是我国古代四大发明之一,爆炸时发生的反应的化学方程式为



。该反应所涉及的下列物质中,元素化合价标注正确的是( )
-
8.
“克劳斯法”是处理含硫废气和回收硫资源的重要方法之一,该方法可减缓二氧化硫对大气的污染,反应的微观过程如图所示。下列说法正确的是( )

A . 该反应中分子、原子种类均发生改变
B . 参加反应的两种分子的个数比为1:3
C . 反应后催化剂的质量减少
D . 该反应可减少酸雨的产生
-
9.
有X、Y、Z三种金属,X和稀盐酸不反应,Y和稀盐酸反应有气泡产生,X放入AgNO3 , 溶液中表面有银白色固体出现,Z与AgNO3溶液无明显现象,则X、Y、Z三种金属的活动性由弱到强的顺序是( )
A . X<Z<Y
B . Z<Y<X
C . Z<X<Y
D . Y<X<Z
-
10.
在给定条件下,下列物质间的每一步转化,均能通过一步反应实现的是( )
-
11.
物质的鉴别和除杂是重要的实验技能。下列实验方法能达到目的的一项是( )
选项 | 实验目的 | 实验方法 |
A | 鉴别羊毛纤维和棉纤维 | 灼烧,闻气味 |
B | 鉴别钾肥和磷肥 | 加熟石灰研磨 |
C | 除去高锰酸钾中的锰酸钾 | 加热固体混合物 |
D | 除去Na2SO4溶液中的少量CuSO4 | 加入过量的氢氧化钠溶液 |
A . A
B . B
C . C
D . D
-
12.
熟石灰广泛用于生产农药、漂白剂、其溶解度曲线如图所示。下列有关说法正确的是( )
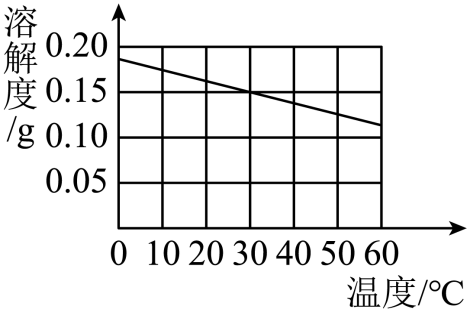
A . 熟石灰易溶于水
B . 熟石灰溶液的pH<7
C . 30℃时熟石灰溶液的溶质质量分数 D . 60℃的熟石灰溶液降温至20℃,溶液变浑浊
D . 60℃的熟石灰溶液降温至20℃,溶液变浑浊
-
13.
如图,室温时,盛水的烧杯内放置两支分别盛有等质量KNO
3溶液和饱和石灰水的试管甲和乙,烧杯的水中漂浮小木块丙。向烧杯内的水中加入氢氧化钠固体后,下列说法正确的是( )
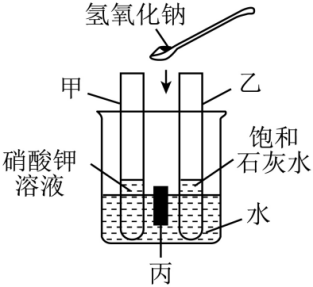
A . 甲中溶液一定为不饱和溶液
B . 甲、乙中溶液质量相等
C . 乙试管中无明显现象
D . 小木块丙会下沉
-
14.
工业上炼铁的原理是一氧化碳和氧化铁反应。某兴趣小组利用如图所示的微型装置进行一氧化碳和氧化铁反应的实验。下列说法正确的是( )

A . 实验时应先点燃酒精喷灯,后将注射器内的一氧化碳推入硬质玻璃管中
B . 实验过程中观察到黑色固体逐渐变红
C . 实验中观察到滤纸条变蓝,说明有二氧化碳生成
D . 气球的主要作用是防止尾气逸出污染空气
-
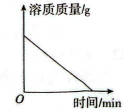
A . ①表示将一定量的60℃硝酸钾饱和溶液冷却至室温
B . ②表示向相同质量和相同质量分数的稀盐酸中,分别加入过量Mg(OH)2和MgO固体
C . ③表示向一定量的稀盐酸和氯化铜的混合溶液中,逐滴加入过量的氢氧化钠溶液
D . ④表示将等质量的铁粉和锌粉同时分别放入两份溶质质量分数相同的足量稀盐酸中
二、填空题(本大题共5小题,每空2分,共30分。)
-
16.
春节期间,龙江冰雪旅游爆火“出圈”,来自五湖四海的游客,在冰天雪地中赏冰乐雪,美丽的哈尔滨更受游客喜爱。地铁二号线贯穿大多数市内著名景点,极大地方便了游客出行。地铁在行驶过程中的能量是由能转化为机械能。传统燃油车使用的燃料来自于分馏,石蜡也是分馏的产物之一,石蜡中含有碳元素和氢元素,则蜡烛充分燃烧会生成。
-
17.
第19届亚运会在杭州顺利举办,主火炬使用的燃料为甲醇(CH3OH),是将焦炉气中的氢气与工业尾气中的二氧化碳在催化条件下反应而制得,同时产生水。由于制备和燃烧过程中,二氧化碳的净排放为零,因此被称为“零碳甲醇”。
-
-
-
(3)
杭州亚运会各场馆的所有电力供应均为“绿电”,“绿电”的主要来源为新能源。下列可作为“绿电”来源的是____(填序号)。
A . 风能
B . 煤炭
C . 太阳能
-
18.
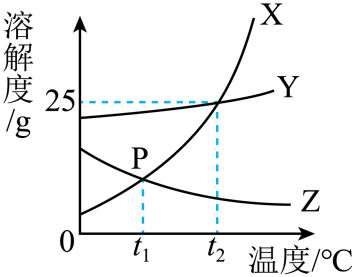
X、Y、Z三种固体物质的溶解度曲线如图所示。请回答:
-
-
(2)

℃时,50g

与25gX混合,所得溶液是
(填“饱和溶液”或“不饱和溶液”)
-
(3)
将

℃时X、Y和Z三种物质的饱和溶液分别升温至

℃,有晶体析出的是
。
-
19.
已知A、C均为单质,且A是年产量最高的金属,C是气体;B、D、E均为氧化物,其中D是黑色固体,B与E的组成元素相同且B有剧毒。它们之间的关系如图所示。(“—”表示能发生反应,“→”表示反应一步完成;部分反应物、生成物及反应条件已略)

-
-
-
-
20.
废弃的镍锌电池中含有锌、铜、银、镍四种金属。为探究镍的金属活动性顺序并回收银,某校化学兴趣小组的同学设计了如图实验流程(反应条件已略去)。已知镍的相对原子质量为59。

-
-
-
(3)
向固体A中加入一定量的AgNO3 , 溶液后发生反应的化学方程式为。
-
(4)
由该实验可知,锌、铜、银、镍的金属活动性顺序由大到小为。
三、实验与探究题(本大题共2小题,每空2分,共20分。)
-
21.
如图是实验室常见的气体制取装置。

-
-
(2)
实验室制取二氧化碳气体的化学方程式为
,若收集干燥的二氧化碳可向图1的

装置中添加液体药品
(填名称)达到干燥气体的目的,二氧化碳应从
(填“

”或“

”)端进入

装置中。
-
(3)
图2是根据图1设计的简易制氧机简图,下列说法正确的是____(填字母)。
A . 制取氧气过程中洗气室压强减小
B . 通过洗气室中的水可观察输出氧气的速率
C .  剂和
剂和 剂可能为过氧化氢溶液和二氧化锰
剂可能为过氧化氢溶液和二氧化锰
-
22.
(2022·灌南模拟)
某小组同学利用如图所示装置检验某气体a的成分。已知a中含水蒸气、氯化氢、甲烷、氢气中的一种或几种(夹持仪器未画出,假设每步反应均完全)。
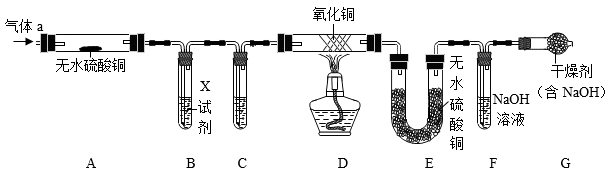
已知:
I.无水硫酸铜粉末遇水由白色变蓝色。
Ⅱ.①  ;②
;② 
-
-
(2)
若X试剂为硝酸银溶液,观察到澄清溶液变浑浊,则证明该气体中含有HCl,写出该反应的化学方程式为。为证明气体中含有HCl,还可以将试剂X换成。
-
-
(4)
若反应后装置E、F分别增重4.58、4.4g,据此可以确定a中一定含有。
-
四、计算题(共5分)
-
23.
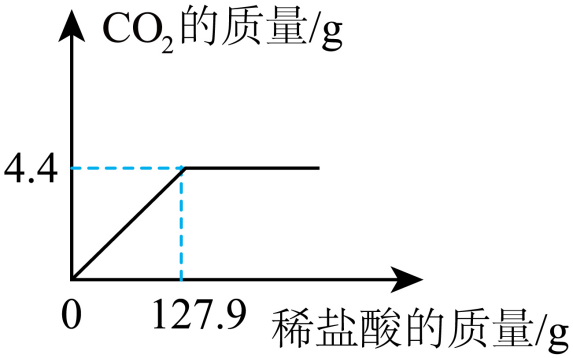
学校项目学习小组到超市买了一包碱面,包装袋上标明主要成分是碳酸钠(Na
2CO
3),还含有少量的氯化钠(NaCl)。该兴趣小组为研究其成分,称取样品12.5g放入烧杯中,再向其中逐滴加入127.9g稀盐酸,反应生成二氧化碳的质量与所加入的稀盐酸的质量关系如图所示。请计算:
-
-
 ②
② ③
③ ④
④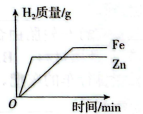

;②