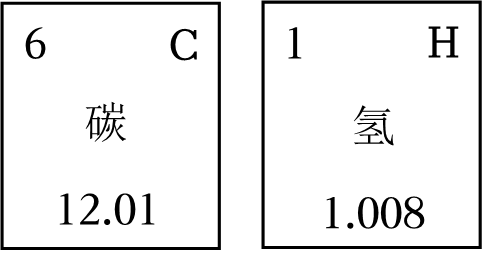
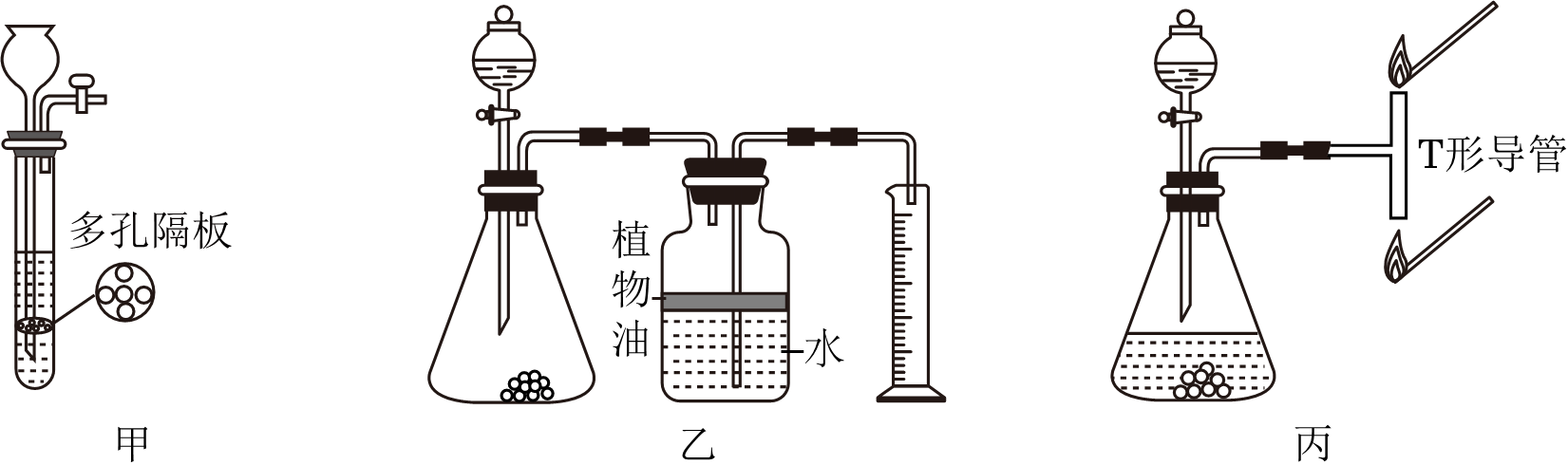
玻璃导管口燃着的木条熄灭,由此可知CO2所具有的化学性质为 。
【查阅资料】
①茶垢清洁剂的主要成分为过碳酸钠(2Na2CO3•3H2O2);
②过氧化氢溶液可以使变红色的酚酞溶液褪色;
③MnO2与Na2CO3、CaCl2均不反应。
【提出问题】茶垢清洁剂与水反应后的产物中含有什么?
【进行猜想】猜想:Na2CO3和H2O2。
步骤 | 操作 | 现象 | 结论 |
1 | 向试管中加入足量CaCl2溶液 | 产物中含有Na2CO3 | |
2 | 再向试管中加入少量MnO2 , 然后把带火星的木条伸入到试管中 | 产生大量气泡,带火星的木条复燃 | 产物中含(填化学式) |
【交流讨论】
老师提出:步骤1中是否可以用无色酚酞溶液来检验Na2CO3的存在?小福认为不可行,原因是 ;小田表示,若更换步骤1、步骤2的实验顺序,则可行,原因是 。
结合上述实验事实,你对于保存茶垢清洁剂提出的建议是 。


小雪认为该低钠盐溶液呈酸性,她的判断依据是 。