⑴只带一个单位电荷(正、负电荷),则把个数“1”省去,直接在元素符号右上角写“+”或“-”号,如 Na+、Cl-等。
⑵带多个单位电荷(正、负电荷),则在元素符号右上角先写电荷数,再写“+”或“-”.号,如 Mg²+、Al³+、O²-等。
⑶较为复杂的离子:有些离子的组成不止一种元素,如OH-和SO4²-等,这种离子称为某某根离子,这些离子是带电的原子团。常见的带电原子团有:
离子名称 | 离子符号 | 离子所带电荷 |
硫酸根离子 | SO42- | |
碳酸根离子 | CO32- | -2 |
碳酸氢根离子 | HCO3- | |
硝酸根离子 | NO32- | -1 |
氢氧根离子 | OH- | -1 |
铵根离子 | NH4+ | +1 |
磷酸根离子 | PO43- | -3 |
说明原子团右上角的数字表示的是整个原子团所带的电荷,而不是某个原子所带的电荷。
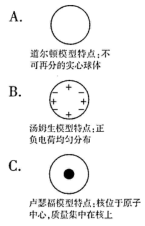
材料一:1803年,道尔顿在原子论中提出:元素由微小的不可分的原子组成;不同元素的原子以简单数目比例形成不可再分的原子——“复杂原子”。
材料二:1809年,盖·吕萨克认同道尔顿的原子论,并提出自己的假说:在同温同压下,相同体积的不同气体中含有相同数目的原子(包括“复杂原子”)。道尔顿反对盖·吕萨克的假说,他认为若该假说成立,解释化学反应时,有些反应会推导出“半个原子”,与原子论矛盾。
材料三:1811年,阿伏加德罗提出分子学说,解决了道尔顿和盖·吕萨克的矛盾。随后科学家们确立并逐步完善了“原子—分子”学说。
【情景提供】19世纪以前,人们一直以为原子是不可分的,直到1897年,汤姆生发现了带负电的电子后,才引起人们对原子结构模型的探索。
【提出问题】电子带负电,原子不带电,说明原子内存在着带正电荷的部分,它们是均匀分布还是集中分布的呢?
【进行实验】1911 年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。
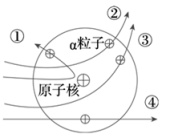
实验做法如图所示:
⑴放射源————放射性物质放出α粒子(带正电荷),质量是电子质量的 7000倍。
⑵金箔———作为靶子,厚度 1μm,重叠了3000层左右的原子。
⑶荧光屏————α粒子打在上面发出闪光。
⑷显微镜————通过显微镜观察闪光,且通过360度转动可观察不同角度α粒子的到达情况。
![]()
【收集证据】绝大多数α粒子穿过金箔后仍沿原来的方向前进,但是有少数α粒子却发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达到180°,像是被金箔弹了回来。
【猜想与假设】α粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。
【解释与结论】