B .
B .  C .
C .  D .
D . 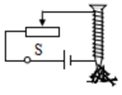

|
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
6 C 碳 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
|
14 Si 硅 28.09 |
15 磷 30.96 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |

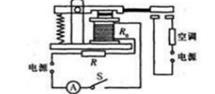
①通过a、b操作,说明感应电流的方向与方向有关。
②通过a、c操作,说明感应电流的方向与方向有关。

①用笔画线代替导线完成图乙中实验器材的连接。(要求滑片向左移动时,电动机的转速变小)
②若开关闭合,线圈不转,用手轻轻一拨,线圈就转动起来,则原来线圈不转的原因可能是。
[情境提供]19世纪以前,人们一直以为原子是不可分的,直到1897年,汤姆生发现了带负电的电子后,才引起人们对原子结构模型的探索。
[提出问题]电子带负电,原子不带电,说明原子内存在着带正电荷的部分,它们是均匀分布还是集中分布的呢?
[进行实验]1911年英国科学家卢瑟福进行了著名的a粒子轰击金属箔的实验。如图所示:
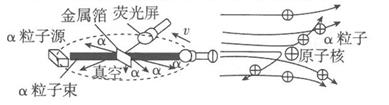
①放射源——放射性物质放出 a粒子(带正电荷),质量是电子质量的7 000倍;
②金属箔——作为靶子,厚度 1 μm,重叠了3 000层左右的原子;
③荧光屏——α粒子打在上面发出闪光;
④显微镜——通过显微镜观察闪光,且通过360度转动可观察不同角度α粒子的到达情况。
[收集证据]绝大多数α粒子穿过金属箔后仍沿原来的方向前进,但是有少数α粒子却发生了较大角度的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达180°,像是被金属箔弹了回来。
[猜想与假设] α粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构。上,否则大角度的散射是不可能的。
[解释与结论]
 道尔顿模型特点:不可再分的实心球体
B .
道尔顿模型特点:不可再分的实心球体
B . 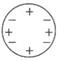 汤姆生模型特点:正负电荷均匀分布
C .
汤姆生模型特点:正负电荷均匀分布
C .  卢瑟福模型特点:核位于原子中心,质量集中在核上
卢瑟福模型特点:核位于原子中心,质量集中在核上
|
原子种类 |
质子数 |
中子数 |
核外电子数 |
相对原子质量 |
|
氢 |
1 |
0 |
1 |
1 |
|
碳 |
6 |
6 |
6 |
12 |
|
氧 |
8 |
8 |
8 |
16 |
|
钠 |
11 |
12 |
11 |
23 |
|
镁 |
12 |
12 |
12 |
24 |
小光:原子里质子数等于核外电子数。
小红:相对原子质量=质子数十中子数。
小伟:原子都是由质子、中子和核外电子构成的。
老师听了三位同学提出的观点后说:“大家总结得非常好,都开动了脑筋,体现了良好的求知态度。
但有一位同学的结论不准确,需要加以修正,而且表中还隐藏着其他的一些结论。
请你认真分析三位同学的观点,并对照上表回答下列问题。
×××补钙剂
[主要原料] 碳酸钙、氧化镁、硫酸锌、硫酸铜、维生素等
[含量] 每片含钙280 mg,镁99.7 mg,锌3.08 mg,铜0.51 mg
[用量] 每日2次,一次1片
甲
葡萄糖酸钙片
[主要原料] 葡萄糖酸钙(C12H22O14Ca)0.5 g
相对分子质量:430
[用法] 口服
[用量] 每日3次,一次?片
乙
请回答下列问题。
|
温度t/℃ |
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
40 |
|
电阻R/Ω |
600 |
550 |
500 |
450 |
420 |
390 |
360 |
330 |
300 |