 B . 滴加液体
B . 滴加液体 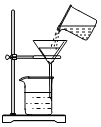 D . 倾倒液体
D . 倾倒液体 
| 选项 | 生活中的现象 | 解释 |
| A | 气体易被压缩 | 因为气体分子间隔很小 |
| B | 在花园中可闻到花的香味 | 因为分子在不断运动 |
| C | 热胀冷缩 | 因为分子大小随温度而改变 |
| D | 水结成冰 | 因为分子发生了变化 |


①2022年6月5日,搭载神舟十四号载人飞船的长征二号F遥十四运载火箭成功发射。陈冬、刘洋、蔡旭哲也是2022年载人航天飞船工程项日迈进太空站修建环节后,我国第一批宣布进驻“龙宫”的宇航员。该运载火箭的推进剂中有液氢和液氧。试写出氢气在氧气中燃烧的符号表达式:。
②空间站的桁架的两端安装了数对大型的太阳能电池板,它们是国际空间站动力和能源的主要提供装置。太阳能电池板的基板材料玻璃纤维中含有多种成分,其中有Na2SiO3、CaSiO3、SiO2。在上述三种物质中,硅元素的化合价均为。
①在如图所示的微观示意图中,能表示化合物的是(填字母,下同),能表示3个分子的是;能表示混合物的是;能表示3个原子的是。

②由![]() 构成的物质中,
构成的物质中,![]() 与
与![]() 代表的元素的质量比为。
代表的元素的质量比为。



【提出问题】足量红磷在密闭的四颈平底瓶内燃烧熄灭后,容器中是否有氧气剩余?
【作出猜想】猜想①:有氧气剩余;猜想②:无氧气剩余。
【实验验证】该小组同学按图1组装好实验装置,利用高能激光笔照射燃烧匙上的红磷,红磷燃烧直至熄灭;待装置完全冷却后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被点燃。
在图2中(填“A、B、C、D、E”)点时红磷燃烧熄灭;白磷开始燃烧至燃烧结束对应的曲线为段(用图2中字母表示)。