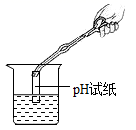
 B . 取固体药品
B . 取固体药品 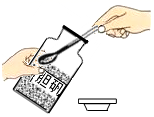 C . 熄灭酒精灯
C . 熄灭酒精灯 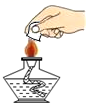 D . 过滤
D . 过滤 
中国白酒主要是以高粱、小麦等谷物为原料的蒸馏酒。白酒的“度数”是指室温下酒中酒精(乙醇 CH3CH2OH)所占的体积百分比。“53 度 ”就表示在 100 毫升的酒中,有 53 毫升酒精。
白酒有一个重要指标,叫做“口感醇厚”,一般用“粘度”来进行衡量,粘度越大口感越醇厚。“粘度”取决于液体中分子的种类及分子之间的相互吸引力。酒精度数与酒粘度呈现出曲线关系,如图 1。

饮入体内的酒精 90% 到达肝脏进行代谢,肝脏就像一个大化工厂,其中有多种渠道帮助酒精变身。酒精变身后产生的乙醛有毒性,能够破坏身体内某些蛋白质,对人体的肝脏和胰脏影响很大。酒精进入身体后,10 分钟就能到达大脑,长久作用对大脑有很大毒害。

医用酒精的主要成分也是乙醇,生产过程与白酒相似,但酒精度数高,除乙醇外,还含有醚、醛等成分,所以不能饮用,但可接触人体杀菌消毒。某科研小组在其他条件相同时, 测量不同浓度的酒精溶液杀灭某病菌所需要时间,实验结果如上图 2 所示。
回答下列问题:
资料:一般条件下,氯气是黄绿色、有刺激性气味的气体,且不燃烧、不支持燃烧。
猜想I:该气体可能是氧气。
实验1:取少量84消毒液于试管中,再加入H2O2溶液,快速伸入带火星的木条。
实验现象:。.
结论1:说明猜想I成立,产生的气体是氧气。
实验2:向锥形瓶中加入35mL84消毒液,注射器中吸入30mL5%的H2O2溶液,并将其平均分6次推入锥形瓶中,每次推入5mLH2O2溶液,待不再产生气泡后,记录所得气体的体积(见下表)。

| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 收集气体的总体积/mL | 140 | 280 | 365 | 370 | 375 | x |
结论2:分析表中的数据可以说明,猜想II(填“成立”或“不成立”)。依据是。
反思:将84消毒液和H2O2溶液混合使用并不能使消毒效果更好,两者发生化学反应反而会使消毒效果变差。