步骤 | 实验内容和操作 | 实验现象 | 结论 |
① | 将适量过碳酸钠固体溶于水 | 无色溶液 | |
② | 将上述溶液加入盛有二氧化锰固体的试管,试管门放置带火星的木条。 | 有气泡生成,带火星的木条复燃 | 生成的气体是 |
③ | 待上述反应完全后,将上层清液分为三份。取第一份清液,用洁净的铂丝蘸取后,在火焰上加热 | 火焰的颜色为 | 溶质中含有钠元素 |
④ | 取第二份清液于试管中,滴加(填试剂的名称) | 无色溶液变为红色 | 溶液呈碱性 |
⑤ | 取第一份清液于试管中,滴加足量盐酸 | 有气泡生成 | 溶质中含有(填原子团的名称) |

温度 | 20℃ | 50℃ | 70℃ | |
溶解度(g/100g水) | 氯化钠 | 36 | 37 | 37.8 |
硫酸镁 | 33.5 | 49 | 37.8 | |
七水合硫酸镁 | 106 | 207 | 253 |
表1
①硫酸镁的溶解度曲线是(请字母编号)。
②50℃的饱和氯化钠溶液质量分数为。
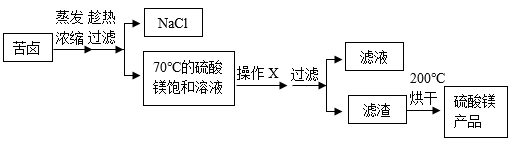
资料:硫酸镁从溶液中析出时会带有结晶水形成七水合硫酸镁晶体,200℃烘干能使其完全失去结晶水。
水 | 氯化钠 | 硫酸镁 |
100g | 36g | 24g |
表2
方案一:
方案二:
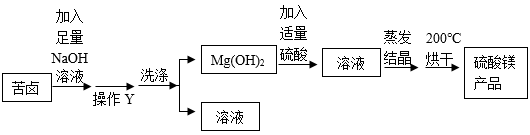
①操作X、操作Y的名称分别是,。
②方案中有酸和碱发生的反应,写出该反应的化学方程式。
③方案二中若要使160g苦卤完全沉淀出Mg(OH)2 , 根据化学方程式计算至少要加多少摩尔NaOH?。
④若两套方案使用相同质量的苦卤进行生产,请比较产品中硫酸镁的质量:m(方案一)m(方案二)。(填“<”、“>”或“=”)
⑤请从产品纯度角度分析、比较两套方案。
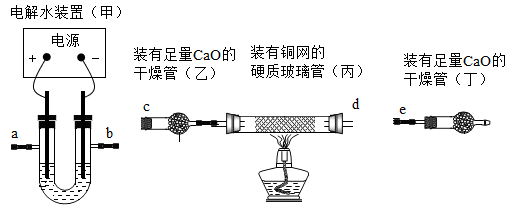
①请写出电解水的化学方程式。
②连接ac,打开电源,点燃酒精灯,一段时间后,丙中观察到的现象为。
③熄灭酒精灯,断开ac,冷却装置待用。
装置编号 | 甲 | 乙 | 丙 | 丁 |
反应前后的质量差(单位:g) | m1 | m2 | m3 | m4 |
①要达到测定目的,必须称量的装置为。(填写装置编号)
②实验时,打开电源,过段时间后,再点燃酒精灯的目的是。写出丙装置中发生反应的化学方程式。
③实验测得数值要与理论值作比较,理论上水中氢、氧元素质量比:。
④若其他操作无误,在实验结束时的操作为熄灭酒精灯→拆卸装置→冷却后称量,则实验测得水中的氢、氧元素质量比的数值会有怎样的变化?并解释原因。。