①2g氢气在8g氧气中充分燃烧,生成10g水
②粗盐通过溶解、沉淀、过滤、蒸发、结晶的处理,得到纯净的盐
③不加任何试剂就能鉴别MgCl2溶液、NaOH溶液、稀硫酸、FeCl3溶液、NaNO3溶液
④如图1所示,锥形瓶中有固体A,胶头滴管有液体B,能使气球膨胀的A、B物质组合可以是生石灰和水、氢氧化钠和水、锌和稀盐酸、氢氧化钙和稀盐酸、硝酸铵和水
⑤向盛有硫酸和硫酸铜混合溶液的烧杯中滴入Ba(OH)2溶液,烧杯中溶质的质量与加入的Ba(OH)2溶液的质量关系如图2所示,则b点时溶液中溶质为硫酸铜


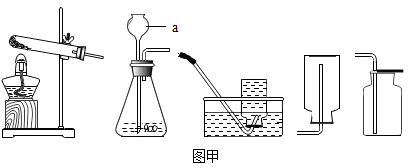
①实验结束后,理论上管a和管b中收集到的气体体积比为,管中的气体具有可燃性。
②实验能够得出的结论是:水是由组成的。
|
矿石名称 |
赤铁矿 |
孔雀石 |
辉铜矿 |
铝土矿 |
白钨矿 |
|
图样 |
|
|
|
|
|
|
主要成分 |
Fe2O3 |
Cu2(OH)2CO3 |
Cu2S |
Al2O3 |
CaWO4 |
①铁矿(主要成分:Fe2O3)和铝土矿(主要成分:Al2O3)是工业炼铁、炼铝重要的金属矿石,请判断Fe2O3和Al2O3属于(填“单质”或“化合物”)。
②金属如铁块可以压成铁片,抽成丝,是利用了金属的性。
③我国古代曾用“湿法炼铜”、“火法炼铜”。“湿法炼铜”的原理是“曾青(硫酸铜溶液)得铁则化为铜”;“火法炼铜”中用辉铜矿(主要成分:Cu2S)炼铜的原理是:Cu2S与氧气在高温条件下反应生成铜和一种会导致酸雨的气体(其相对分子质量为64)。请写出“火法炼铜”的化学方程式。
④保护金属资源的途径有:防止金属腐蚀、金属的回收利用、合理开采矿物、。
A.盐酸 B.熟石灰 C.烧碱 D.小苏打
①用于改良酸性土壤的是。
②用于金属除锈的是。
③用于焙制糕点的是。
④炉具清洁剂中含有的是。
2022年2月2日上午,北京2022年冬奥会火炬接力启动仪式在北京奥林匹克森林公园举行。火炬“飞扬”传递过程中,不怕大风、不惧严寒。“飞杨”总重量1.1kg,能抵抗-40℃的低温,防水性能良好。“飞扬”火炬外壳采用碳纤维材料来代替传统的金属材料,轻而强是碳纤维最大的特点,其密度只有钢的四分之一,强度却是钢的6~7倍。“飞扬”采用的是氢燃料,该设计体现了绿色办奥理念和科技冬奥成果。图为充分燃烧1kg天然气、煤和氢气所产生的CO2和SO2 , 气体的质量,表为相同条件下,1g燃料完全燃烧释放的热量。

燃料 | 天然气 | 煤 | 氢气 |
热量(kJ) | 55.9 | 29.3 | 143 |
①前人们使用的燃料大多来自化石燃料,包括煤、石油、,而冬奥会的“飞扬”火炬采用的氢燃料相比于化石燃料的优点是(一条即可)。
②火炬外壳材料采用的碳纤维属于(填“金属”或“复合”)材料。
③下列做法不符合“绿色”办奥理念的是(填字母)。
A.奥运村食堂提供聚乳酸生物可降解餐具
B.乘坐公共交通工具前往奥运场馆
C.颁奖采用永不凋谢的绒线花
D.为增加气氛大量燃放烟花爆竹


①实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中黑色固体变为红色,由此判断热分解产物中一定含有。
②装置中B、C、D的作用分别是。(填字母)
A.检验CO2、吸收CO2、吸收水分
B.吸收CO2、检验CO2、吸收水分
③请写出装置C中发生反应的化学方程式。

②当观察到甲试管中出现的现象时,说明甲试管中两种物质恰好完全反应;
③乙试管中两种溶液不能发生反应,理由是。
【提出问题】废液缸中上层液体的溶质成分有哪些?(酚酞除外)
【作出猜想】
猜想一:NaCl、NaOH
猜想二:NaCl、NaOH、BaCl2
猜想三:
实验步骤 | 实验现象 | 实验结论 |
取少量废液缸中上层液体于试管中,加入溶液,充分反应。 | 猜想三成立 |