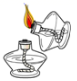
 B . 测定溶液pH值
B . 测定溶液pH值  C . 闻药品气味
C . 闻药品气味  D . 倾倒液体
D . 倾倒液体 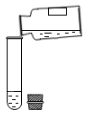

方法一:火法炼铜:
方法二:湿法炼铜:
上述两种方法中,你认为方法(填“一”或“二”)更好,原因是(写两点即可)。


【查阅资料】
Ⅰ、
Ⅱ、
Ⅲ、CaO2·8H2O在水中不太稳定,会缓慢分解。
①平均反应速率最快的时间段为:(填字母)。
a.0~10 min b.10~20 min c.20~30min d.30~40 min
②30min后,w开始下降的主要原因是。
项目一:探究固体酒精的成分
【查阅资料】
①固体酒精是将酒精、NaOH等按一定质量比混合制成。【进行实验】同学们取少量固体酒精于试管中,加入足量蒸馏水,振荡,向其中滴加酚酞溶液,观察到溶液变为红色。小米很肯定地告诉大家,固体酒精中含有NaOH。
|
实验步骤 |
实验方法 |
实验现象 |
实验结论 |
|
步骤一 |
取少量该固体酒精,向其中加入足量蒸馏水,搅拌 |
固体酒精部分溶解 |
|
|
步骤二 |
取上层清液,向其中滴加,振荡 |
有白色沉淀产生 |
该固体酒精中含。 |
|
步骤三 |
取步骤二所得的上层清液于试管中,向其中滴加硫酸铜溶液,振荡 |
有蓝色沉淀产生 |
该固体酒精中含NaOH |