
该学生观察到如下化学现象:装置A中澄清的石灰水变白色浑浊,装置B中白色无水硫酸铜变蓝,装置C中浓硫酸无明显变化,装置D中黑色的氧化铜变为一种亮红色物质,装置E中澄清的石灰水变白色浑浊,装置F中白色的无水硫酸铜变蓝色。该学生从上述实验现象中得出如下结论:气体中① 肯定不含CO2;② 肯定含CO; ③ 肯定含H2O(气);④ 肯定含H2;⑤ 可能含N2。
小红发现,金店里有两种不同的“白金”,单价相差悬殊,小红很好奇,打算进行研究。
【查阅资料】市场上所谓的“白金”通常有两种,一种是金、镍、铜、锌的合金,称为白色金;另一种是铂金,铂是一种银白色的贵重金属,用于耐腐蚀的化学仪器及首饰等,俗称“白金”−元素符号Pt。小红结合化学课上学习的金属活动性顺序,展开了下列实验活动。
探究Zn、Ni(镍)、铜的活动性顺序。
【作出假设】对三种金属的活动性顺序提出可能的假设:①Zn>Ni>Cu;②Zn>Cu>Ni;你觉得还有其他的可能性吗?请把它们写出来(一种即可)。
|
OH− |
NO3− |
SO42− |
Cl− |
|
|
Ni2+ |
不 |
溶 |
溶 |
溶 |
【设计实验】同温下,取大小、厚度相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象。
【记录现象】请帮助小红把实验现象填写完整
|
金属 |
Ni |
Zn |
Cu |
|
与盐酸反应的现象 |
气体产生缓慢,金属逐渐溶解 |
气体产生迅速,金属迅速溶解 |
|
式。
实验过程:
①取少量废水加入过量的盐酸,有白色沉淀生成,过滤,得沉淀物和滤液。向沉淀中加入稀硝酸白色沉淀不溶解。
②将所得滤液分成两份,一份滤液中加入适量的稀硫酸产生白色沉淀,过滤,向沉淀物中加入稀硝酸沉淀不溶解。
③向另一份滤液中加入过量氢氧化钠溶液,只产生蓝色沉淀。
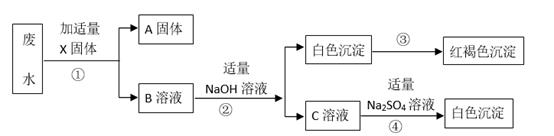
X固体为
|
实验次数 |
1 |
2 |
3 |
4 |
5 |
|
加入稀盐酸的质量/克 |
20 |
20 |
20 |
20 |
20 |
|
剩余固体的质量/克 |
8.0 |
6.0 |
4.0 |
2.2 |
2.2 |
回答下列问题:
新型铸铁材料−−蠕墨铸铁在高碳铁液中加入稀土合金,得到断口呈“花斑”状,石墨为蠕虫状蠕墨铸铁(又称蠕铁)。蠕铁是具有片状和球状石墨之间的过渡形态铸铁,片状石墨和球状石墨内部原子排列方式不同。蠕铁是一种具有良好力学性能(耐高温、强度大、断面敏感性小)、导热率高和抗氧化性能的新型铸铁材料。蠕铁广泛用于制造汽车发动机、汽车制动零件、排气管等。国产蠕铁中的蠕化剂均含有稀土元素,如稀土硅铁镁合金、稀土硅钙合金等。国产蠕铁技术冲破了国外的技术封锁,助推我国发动机制造技术迈向世界领先水平。
回答下列问题: