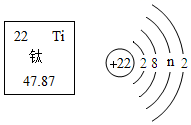
A 钛原子在化学反应中易失去电子 B 图中n的值为10
C 钛原子的中子数为22 D 钛原子的相对原子质量为47.87g
A 凡是均一、稳定的液体一定是溶液
B 饱和溶液不能再溶解任何物质
C 对于同种溶质,在相同条件下时,饱和溶液比不饱和溶液浓
D 氢氧化钠溶于水形成溶液时,温度下降
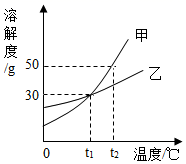
①t1℃时,溶解度大小关系:甲乙(填“>”“<”或“=”);
②t2℃时,等质量的甲、乙饱和溶液中溶剂质量关系:甲乙(填“>”“<”或“=”);
③当甲中混有少量的乙时,提纯甲所用的方法为。

①CaO ②AgNO3 ③CO ④CO2
|
操作 |
| | | |
| 现象 | 产生少量气泡 | 产生大量气泡 |
| 无明显实验现象 |
①同学们经过讨论后认为:上述方案可以优化,(填“甲”“乙”“丙”或“丁”)试管的实验是多余的。
②某同学认为,只用一支盛有少量稀硫酸的试管,合理安排金属片的插入顺序(能与稀硫酸反应的要一次性将稀硫酸消耗完),也能证明锰、锌、铜这三种金属的活动性顺序。
他设计了两种插入顺序,请你补全顺序二:
顺序一:Cu、Mn、Zn;
顺序二:(填化学式,下同)。
(查阅资料)
①发热包的主要成分为氧化钙、活性炭、铝粉、铁粉、碳酸钠。
②
③铝能与氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和氢气。
取出发热包加入凉水,剧烈反应,放出大量热,产生该现象的化学方程式为。反应结束后,烧杯底部有大量固体,继续加水搅拌,过滤、洗涤、干燥,得到固体混合物。
固体混合物的成分可能有:活性炭、铝粉、铁粉、碳酸钙。为进一步探究其成分,某小组同学设计并进行如下实验:
|
实验操作 |
实验现象 |
结论 |
|
|
① |
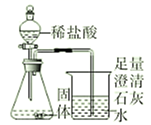
取少量固体于锥形瓶中,逐渐加入稀盐酸至不再产生气泡为止(如图所示) |
瓶底有黑色固体剩余 |
黑色固体为 |
|
溶液 |
固体中含有铁粉 |
||
|
澄清石灰水变浑浊 |
固体中含有碳酸钙 |
||
|
② |
另取少量固体于试管中,加入足量溶液 |
产生大量气泡 |
固体中含有铝粉,反应的化学方程式是 |
A 发热包应密封防潮保存
B 能与水混合放出热量的物质均可做发热包的发热材料
C 使用后的发热包应包好按照垃圾分类标准投放
你认为其中正确的是(填标号)。